
【题目】以NaCl等为原料制备KClO4的过程如下: ①在无隔膜、微酸性条件下,发生反应:NaCl+H2O﹣NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3 .
③一定条件下反应:4KClO3 ![]() 3KClO4+KCl,将产物分离得到KClO4 .
3KClO4+KCl,将产物分离得到KClO4 .
(1)电解时,产生质量为2.13g NaClO3 , 同时得到H2的体积为L(标准状况).
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是 .
(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验: 准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4﹣全部转化为Cl﹣(反应为:3KClO4+C6H12O6═6H2O+6CO2↑+3KCl),加入少量K2CrO4溶液作指示剂,用0.20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积为21.00mL.滴定达到终点时,产生砖红色Ag2CrO4沉淀.
①已知:Ksp(AgCl)=1.8×10﹣10 , Ksp(Ag2CrO4)=1.1×10﹣12 , 若c(CrO42﹣)=1.1×10﹣4mol/L,则此时c(Cl﹣)=mol/L.
【答案】
(1)1.344
(2)低温时,KClO3溶解度小,从溶液中结晶析出
(3)1.8×10﹣6②计算KClO4样品的纯度(请写出计算过程.)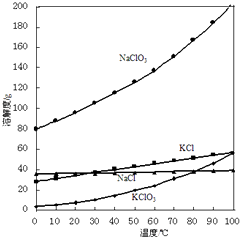
解:准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4﹣全部转化为Cl﹣(反应为:3KClO4+C6H12O6═6H2O+6CO2↑+3KCl),加入少量K2CrO4溶液作指示剂,用0.20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积为21.00mL.
n(AgNO3)=0.2000 mol?L﹣1×0.021L=0.0042 mol,
n(KCl)总=n(AgNO3)=0.0042 mol
n(KClO4)+n(KCl)=0.0042 mol,
n(KClO4)×138.5 g?mol﹣1+n(KCl)×74.5 g?mol﹣1=0.56890g,
n(KClO4)=0.0040 mol,
m(KClO4)=0.004 mol×138.5 g?mol﹣1=0.554g,250ml溶液中m(KClO4)=5.54g
KClO4样品的纯度= ![]() ×100%=97.3%,
×100%=97.3%,
答:n(AgNO3)=0.2000 mol?L﹣1×0.021L=0.0042 mol,
n(KCl)总=n(AgNO3)=0.0042 mol
n(KClO4)+n(KCl)=0.0042 mol,
n(KClO4)×138.5 g?mol﹣1+n(KCl)×74.5 g?mol﹣1=0.56890g,
n(KClO4)=0.0040 mol,
m(KClO4)=0.004 mol×138.5 g?mol﹣1=0.554g,
250ml溶液中m(KClO4)=5.54g
KClO4样品的纯度= ![]() ×100%=97.3%
×100%=97.3%
【解析】解:(1)电解时,产生质量为2.13g NaClO3 , 物质的量= ![]() =0.02mol
=0.02mol
NaCl+3H2O= | NaClO3+ | 3H2↑1 |
1 | 3 | |
0.02mol | 0.06mol |
同时得到H2的物质的量为0.06mol,体积=0.06mol×22.4L/mol=1.344L,
所以答案是:1.344;(2)在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3的原因是低温时,KClO3溶解度小,从溶液中结晶析出,
所以答案是:低温时,KClO3溶解度小,从溶液中结晶析出;(3)①若c(CrO42﹣)=1.1×10﹣4mol/L,Ksp(Ag2CrO4)=c2(Ag+)c(CrO4 2﹣)=1.1×10﹣12 , c(Ag+)=10﹣4mol/L,
Ksp(AgCl)=c(Ag+)c(Cl﹣)=1.8×10﹣10 , c(Cl﹣)=1.8×10﹣6 mool/L,
所以答案是:1.8×10﹣6;


科目:高中化学 来源: 题型:
【题目】小王同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及时制止。原因是CO2可以支持镁燃烧发生以下反应:2Mg+CO2![]() 2MgO+C,下列关于该反应的判断正确的是( )
2MgO+C,下列关于该反应的判断正确的是( )
A. Mg元素化合价由0价升高到+2价,所以MgO是还原产物
B. 由此反应可以判断氧化性CO2>MgO,还原性Mg>C
C. CO2作氧化剂,表现氧化性,发生氧化反应
D. Mg原子得到的电子数目等于碳原子失去的电子数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变化为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
A.氧化性B.还原性C.碱性D.酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列有关化学基本概念的依据正确的是
A. 溶液与胶体:本质区别是能否发生丁达尔效应
B. 纯净物与混合物:是否仅含有一种元素
C. 物理变化与化学变化:是否有新物质生成
D. 电解质与非电解质:物质本身的导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得1mol H2与1mol Cl2反应生成2mol HCl时,放出184.6kJ的热量,其理论分析数据与实验数据略有差异,如图表示上述反应能量变化的理论分析示意图:
(1)化学键断裂需要(填“释放”或“吸收”)能量;
(2)图中表示了吸收和释放的能量,其中释放的能量共kJ;
(3)该反应的反应物的总能量(填“大于”、“等于”或“小于”)反应产物的能量,所以该反应是(填“放热”或“吸热”)反应;
(4)用图示数据计算其反应热,写出该反应的热化学方程式 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL的某稀H2S04溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴人氨水体积变化如图.下列分析正确的是( ) 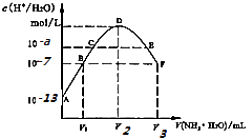
A.稀硫酸的浓度为0.1mol/L
B.C点溶液pH=14﹣a
C.E溶液中存在:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
D.B到D、D到F所加氨水体积一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH 溶液中逐滴加入AlCl3溶液,生成沉淀A1(OH)3的量随AlCl3加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是

A. a点对应的溶液中:Na+、Fe3+、SO42-、HCO3-
B. b点对应的溶液中:Na+、S2-、SO42-、Cl-
C. c点对应的溶液中:Ag+、Ca2+、NO3-、F-
D. d点对应的溶液中:K+、NH4+、I-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com