
【题目】下面的电子运动状态存在的是( )
A.n=1,l=1 m=0
B.n=2,l=0 m=±1
C.n=3,l=3 m=±3
D.n=4,l=3 m=±2
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
【题目】现有金属A、B和气体甲、乙、丙及物质C、D、F、F,它们之间的转化发生如下反应,(图中有些反应的产物和反应条件没有全部标出),黄绿色气体溶于水后的溶液有漂白性且能杀菌消毒,其中物质F的水溶液呈黄色,物质E在氧化剂作用下很容易转化为物质F,F能与物质C的溶液反应生成红褐色沉淀.
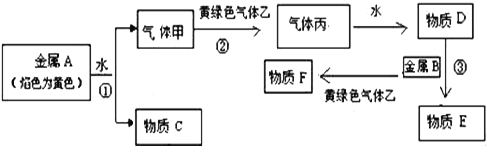
请回答下列问题:
(1)物质F的化学式为______.
(2)①写出金属A与水反应的化学方程式:______.
②写出黄绿色气体乙和水反应的离子化学方式:______.
③实验室制备黄绿色气体的化学方程式:___________.
(3)金属单质A投入到下列溶液中既有气体,又有沉淀出现的是______
A、氯化钠溶液 B、碳酸钠溶液 C、硫酸铜溶液 D、氯化铵溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)主要用于制革、印染、电镀等.其水溶液中存在平衡:Cr2O72﹣+H2O2CrO42﹣+2H+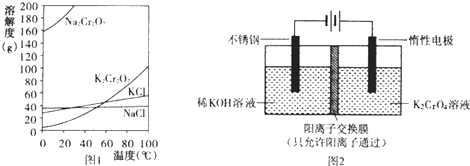
(1)已知有关物质溶解度如图1.用复分解法制备K2Cr2O7的操作过程是:向Na2Cr2O7溶液中加入(填化学式),搅拌溶解,调节溶液pH约为5,加热溶液至表面有少量晶体析出时, , 抽滤得到粗产品,再用重结晶法提纯粗产品.
(2)以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图2.
①不锈钢作极,写出该电极的电极反应式 .
②分析阳极区能得到重铬酸钾溶液的原因 .
③当铬酸钾的转化率达到x时,阳极液中K与Cr的物质的量之比为
(3)铬对环境能造成污染.某酸性废水中含有Cr2O72﹣ , 处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72﹣转化为毒性较低的Cr3+ , 再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mgL﹣1则达到排放标准.
①Na2S2O5参加反应的离子方程式为 .
②经上述工艺处理后的废水,理论上Cr3+浓度约为 mgL﹣1 .
(已知室温下Ksp[Cr(OH)3]≈6×10﹣31)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2C(s)+O2(g)═2CO(g)△H=﹣221.0kJmol﹣1;
②2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1 .
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
A.262.6 kJmol﹣1
B.﹣131.3 kJmol﹣1
C.﹣352.3 kJmol﹣1
D.131.3 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:W、Y、Z、T、M为前四周期元素,且原子半径依次增大.请填空:
(1)W,Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图;
(2)化合物YW3极易溶于水的原因;YW3的分子构型为 . YW3属于(填“极性”或“非极性”)分子,其中Y的化合价为 .
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表周期族.T的化合物TY熔融时不导电,常用作砂轮及耐高温材料,由此推知,它属于(填编号字母);
a.离子晶体 b.原子晶体 c.分子晶体 d.无法判断
(4)M3+的3d轨道为半充满,则M的原子的电子排布式为 , M位于周期表的区(按电子的填入顺序划分),M的晶体中的粒子采用的是体心立方堆积,则该种堆积方式的配位数为 , 若其晶胞的边长为acm,M的摩尔质量为Mr g/mol,阿伏加德罗常数的值为NA , 则其密度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)碱洗铝材除其表面的氧化膜,反应的离子方程式为________________,碱洗时常有气泡冒出,原因是_________________(用离子方程式表示),该反应中的氧化剂是___________。
(2)除去碳酸钠固体中的碳酸氢钠杂质,发生反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 医用酒精的浓度通常是95%
B. 蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N四种元素
C. 淀粉、纤维素和油脂都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A.标准状况下,6.72LO2和N2的混合气体含有的原子数为0.6NA
B.通常状况下,8g O2和O3的混合气体含有的分子数是0.5NA
C.常温常压下,2mol/L的100mL MgCl2溶液中,含有Cl﹣ 个数为0.4NA
D.标准状况下,11.2L He分子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com