
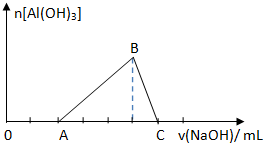
 已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38.向Fe(NO3)3和Al(NO3)3的混合溶液中逐滴加入NaOH溶液,生成Al(OH)3沉淀的物质的量与加入NaOH溶液体积的关系如图所示.计算表明当Fe3+完全沉淀时,Al3+恰好开始沉淀.下列说法正确的是( )
已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38.向Fe(NO3)3和Al(NO3)3的混合溶液中逐滴加入NaOH溶液,生成Al(OH)3沉淀的物质的量与加入NaOH溶液体积的关系如图所示.计算表明当Fe3+完全沉淀时,Al3+恰好开始沉淀.下列说法正确的是( )| A、原混合溶液中c(Fe3+):c(Al3+)=1:1 |
| B、B点两种沉淀共存,此时上层清液中c(Fe3+)=c(Al3+)=0 |
| C、B点两种沉淀共存,此时上层溶液中c(Al3+):c(Fe3+)=2.5×104:1 |
| D、C点溶液中的溶质只有NaAlO2 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、②⑤⑥ | B、②⑥⑦ |
| C、①⑤ | D、③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
| A、(1)(3)(4) |
| B、(2)(3)(5) |
| C、(1)(4)(5) |
| D、(1)(2)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 ),串联变阻器以调节电流,同时标出电极
),串联变阻器以调节电流,同时标出电极查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当酸碱恰好完全中和时,溶液呈中性 |
| B、若溶液中c(H+)与c(OH-)相等,溶液肯定呈中性 |
| C、0.005 mol?L-1 Ba(OH)2溶液中,水电离出的c(OH-)为10-12 mol?L-1 |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、pH=6时,C(H+)=C(SO32-)+C(OH-) |
| B、pH=2时,溶液中存在:C(Na+)>C(HSO3-)>C(H2SO3)>C(SO32-) |
| C、向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中会出现浑浊且pH值降为2,其离子方程式可表示为:Ca2++SO32-═CaSO3 |
| D、由图可知亚硫酸氢钠溶液呈酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com