
对于下列化学反应的实验现象,描述错误的是
[ ]
A.![]() 通入石蕊试液中产生先变红后褪色的现象
通入石蕊试液中产生先变红后褪色的现象
B.铜丝在![]() 气中燃烧生成棕色的烟
气中燃烧生成棕色的烟
C.氢气在氯气中燃烧产生蓝色火焰
D.铜丝在硫蒸气中燃烧生成黑色硫化亚铜
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
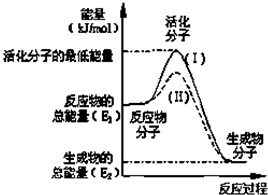 在化学反应中,只有活化分子才能发生有效碰撞而发生化学反应.使普通分子变成活化分子所需提供的平均能量叫活化能,其单位通常用kJ?mol-1表示.请观察如图,回答下列问题:
在化学反应中,只有活化分子才能发生有效碰撞而发生化学反应.使普通分子变成活化分子所需提供的平均能量叫活化能,其单位通常用kJ?mol-1表示.请观察如图,回答下列问题:| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省昆明市官渡区二中高二9月月考化学试卷(带解析) 题型:填空题
(共10分)
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。
①图中所示反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”、“不需要”或“不一定”)加热,该反应的△H = (用含E1、E2的代数式表示)。
②对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子百分数增多,反应速率加快,你认为最可能的原因是____________________________________。
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ ①C(s)+O2(g) === CO2(g) ΔH1<0
途径Ⅱ 先制水煤气:②C(s)+H2O(g) === CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
③2CO(g)+O2(g) === 2CO2(g) ΔH3<0 ④2H2(g)+O2(g) === 2H2O(g) ΔH4<0
请回答下列问题:
①判断两种途径放热:途径Ⅰ放出的热量________途径Ⅱ放出的热量(填“大于”、“等于”或“小于”)。
②ΔH1、ΔH2、ΔH3、ΔH4的数学关系是_________________________________。
③由于制取水煤气的反应里,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________能量才能转化为生成物,因此其反应条件为________。
(3)已知:Fe2O3(s)+3CO(g) === 2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g) === 2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g) === 3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1 ③
请写出CO还原FeO的热化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届云南省昆明市高二9月月考化学试卷(解析版) 题型:填空题
(共10分)
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。

①图中所示反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”、“不需要”或“不一定”)加热,该反应的△H = (用含E1、E2的代数式表示)。
②对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子百分数增多,反应速率加快,你认为最可能的原因是____________________________________。
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ ①C(s)+O2(g) === CO2(g) ΔH1<0
途径Ⅱ 先制水煤气:②C(s)+H2O(g) === CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
③2CO(g)+O2(g) === 2CO2(g) ΔH3<0 ④2H2(g)+O2(g) === 2H2O(g) ΔH4<0
请回答下列问题:
①判断两种途径放热:途径Ⅰ放出的热量________途径Ⅱ放出的热量(填“大于”、“等于”或“小于”)。
②ΔH1、ΔH2、ΔH3、ΔH4的数学关系是_________________________________。
③由于制取水煤气的反应里,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________能量才能转化为生成物,因此其反应条件为________。
(3)已知:Fe2O3(s)+3CO(g) === 2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g) === 2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g) === 3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1 ③
请写出CO还原FeO的热化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学反应中,只有少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应。我们把能引发化学反应的碰撞称为有效碰撞,发生有效碰撞的分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位用kJ•mol-1表示。认真观察下图,然后回答问题。
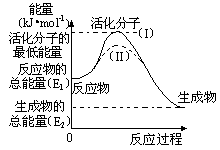 (1)图中反应是 (填“吸热”或“放热”)反应,该反应的△H= (用含E1、E2的代数式表示)。
(1)图中反应是 (填“吸热”或“放热”)反应,该反应的△H= (用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+![]() O2(g) === H2O(g) △H=-241.8kJ•mol-1,该反应的活化能为167.2 kJ•mol-1,则逆反应的活化能为 。
O2(g) === H2O(g) △H=-241.8kJ•mol-1,该反应的活化能为167.2 kJ•mol-1,则逆反应的活化能为 。
(3)对于同一反应,图中虚线(II)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是 。
(4)标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏大的是 。
A.用蒸馏水洗涤锥形瓶后,未干燥就装待测液
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com