
下图分别是金刚石、石墨、C60、碳纳米管结构示意图,说法正确的是( )
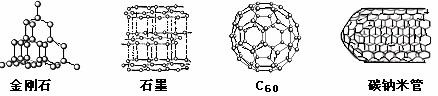
A. 这四种物质都很软,可作润滑剂
B. 这四种物质碳原子的排列方式相同
C. 这四种物质完全燃烧后的产物都是CO2
D. 这四种物质的结构中都是每个碳原子连接3个碳原子
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
Ⅰ.无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾。实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al + 6HCl(g) = 2AlCl3 + 3H2
完成下列填空:
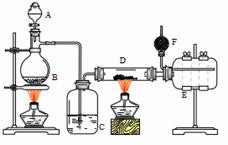
A为浓硫酸,B为NaCl固体
(1)进行实验时应先点燃 (选填“B”或“D”)处酒精灯。
(2)用粗短导管连接D、E的目的是________(选填序号)。
a. 防堵塞 b. 防倒吸 c. 平衡气压 d. 冷凝回流
(3)F中盛有碱石灰,其目的是 (选填序号)。
a. 吸收多余HCl b. 吸收Cl2 c. 吸收CO2 d. 防止空气中H2O进入E瓶
(4)将D中固体改为氯化铝晶体(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是 。若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原氯化铝晶体(AlCl3·6H2O)的40%,则可推算n的值为 。
Ⅱ.焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。Na2S2O5溶于水即生成NaHSO3。
(1)证明NaHSO3溶液中HSO3—的电离程度大于水解程度,可采用的实验方法是 (填序号)。
| a.测定溶液的pH | b.加入Ba(OH)2溶液 | c.加入盐酸 |
| d.加入品红溶液 | e.用蓝色石蕊试纸检测 |
(2)检验Na2S2O5晶体在空气中已被氧化的实验方案是________ ______。
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量的方案如下:

(已知:滴定时反应的化学方程式为SO2 + I2 + 2 H2O = H2SO4 + 2 HI)
按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g/L。在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C三种主族元素,已知A元素原子的价电子构型为nsn,B元素原子的M层上有两个未成对电子,C元素原子L层的p轨道上有一对成对电子,由这三种元素组成的化合物的化学式不可能是
A.A3BC4 B.A2BC4 C.A2BC3 D.ABC4
查看答案和解析>>
科目:高中化学 来源: 题型:
农业技术人员向农民建议:在塑料大棚中种植植物时,可向大棚中通人适量的C02。
这是因为( )
A.C02可使害虫窒息死亡,从而防治病虫害
B.施用二氧化碳能促进植物进行光合作用,提高产量
C. C02可产生温室效应,从而提高大棚内的温度
D. CO2可灭火,施用后防止火灾
查看答案和解析>>
科目:高中化学 来源: 题型:
“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,
溶液的颜色变化情况是 ( )
A. 先变红色后变紫色 B. 变红后颜色不再改变
C. 先变无色后变红 D. 先变蓝色后变紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室里制备和收集氧气、二氧化碳等气体的仪器装置图(图中A~E是仪器
装置代号),请回答下列问题。
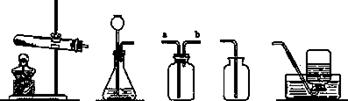
A B C D E
(1)将装置A和E连接,可用于制取_______,将装置B和D连接,可用于制取______;
(2)硫化氢是一种有毒气体,其密度比空气的大,能溶于水。实验室里常用块状固体
硫化亚铁和稀硫酸在常温下反应制取硫化氢气体。可选用_______ ____作气体发生
装置,若收集装置是C,气体由___________(填a或b)导入集气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌

查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E和F六瓶无色溶液,他们是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1) 能确定溶液是(写出溶液标号与相应溶质的化学式):
(2) 不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:

查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成了如下实验:

另取10.80 g X在惰性气流中加热至完全分解,得到6.40 g固体1。请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图:________________。写出气体甲的电子式:________。
(2)X的化学式是________,在惰性气流中加热X至完全分解的化学方程式为__________________________________________________________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是______________________________(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式:_____________________________________________________,并设计实验方案验证该反应的产物:__________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com