
����Ŀ�������£���Cl2����ͨ��100 mLˮ�������ͣ�Ȼ�������ñ�����ˮ����μ���0.1 mol��L��1 NaOH��Һ������������pH�ı仯��ͼ��ʾ�������й�������ȷ����
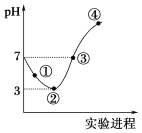
A. ���ߢۢܶ������ӷ�Ӧ��HClO��OH��===ClO����H2O
B. �����ݢڴ����ݼ������ܽ��n(Cl2)
C. �۴���ʾ����������������Һǡ�÷�Ӧ��ȫ
D. �ٴ�c(H��)ԼΪ�ڴ�c(H��)������
���𰸡�A
��������
����A�����ߴ���������ҺpH����˵���˶η�����Ӧ��HCl+NaOH�TNaCl+H2O��HClO+NaOH�TNaClO+H2O�����ӷ�Ӧ�ֱ�Ϊ��H++OH-��H2O��HClO+OH-�TH2O+ClO-�������ʱc��H+��=c��OH-����c��Na+��=c��Cl-��+c��ClO-����HClOΪ������ʣ����ֵ��룬��ʱ��Һ�д��ڴ�����ĵ���ƽ�⣬��������ͼ�������֪����ҺpH����������pH����7���������������ƣ��������ƺʹ����ᷴӦ��HClO+NaOH�TNaClO+H2O�����ɵĴ�������Ϊǿ�������Σ�ˮ��ʼ��ԣ��Ӽ�ֱ�������pH���������������ӷ�ӦΪHClO+OH����ClO��+H2O��A��ȷ��B��������ʾ��Һ�з�����Ӧ��Cl2+H2O![]() H++Cl-+HClO��HClOΪ������ʣ����ֵ��룬������pH����μӷ�Ӧ��������B����C����������������ǡ�÷�Ӧ��ȫ��ҺΪ�Ȼ��ơ�����������Һ����Һ�ʼ��ԣ�������ʾ��Һ�з�����Ӧ��HCl+NaOH�TNaCl+H2O��HClO+NaOH�TNaClO+H2O����Һ�����ԣ�c��H+��=c��OH-����C����D���������������������ܽ�ƽ�⣺Cl2+H2O
H++Cl-+HClO��HClOΪ������ʣ����ֵ��룬������pH����μӷ�Ӧ��������B����C����������������ǡ�÷�Ӧ��ȫ��ҺΪ�Ȼ��ơ�����������Һ����Һ�ʼ��ԣ�������ʾ��Һ�з�����Ӧ��HCl+NaOH�TNaCl+H2O��HClO+NaOH�TNaClO+H2O����Һ�����ԣ�c��H+��=c��OH-����C����D���������������������ܽ�ƽ�⣺Cl2+H2O![]() H++Cl-+HClO���ҽ��еĹ��̣���������ǿ��������Ũ��������D����ѡA��
H++Cl-+HClO���ҽ��еĹ��̣���������ǿ��������Ũ��������D����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Թ�A���ȼ���3 mL��ˮ�Ҵ���Ȼ������Թܱ���������2 mLŨ���ᣬ������2 mL�����ᣬ����ͼװ�ý���ʵ�飬��������������������ͨ���Թ�B�б���̼������Һ��Һ���ϡ���ش��������⣺

��1��Ũ�����������__________________________________________��
��2���Թ�B�й۲쵽��������_____________________________��
��3�����Թ�B�еı���̼������Һ����ˮ���棬ʵ����������ŵ���ζ�Ŀ���ԭ����________________________________________________________________________��
��4���Թ�B�еı���̼������Һ��������__________________________________��
��5��ͨ�������ĵ��ܲ��ܲ����Թ�B��Һ���µ�ԭ����_______________________________________��
��6��ͨ��������ѡ�ó����ܵ�Ŀ����________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̬����ɵĻ��������ȫȼ�պ�����CO2��H2O�����ʵ��������������ʵ����ı仯��ͼ��ʾ�������жԻ�������ж���ȷ���ǣ�
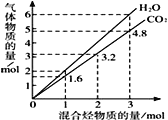
��һ������ϩ ��һ���м��� ��һ���б��� ��һ��û������ݿ����м��� ��������Ȳ��C2H2��
A. �ڢ� B. �ڢۢ� C. �ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�10mL0.40mol/LH2O2��Һ�������ֽ⣬��ͬʱ�̲������O2�����(������Ϊ��״��)���±���������Һ����仯��������������ȷ����( )
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.6 | 16.8 | 22.4 | 26.5 | 29.9 |
A. 2 minʱH2O2��Ũ��c(H2O2)��0.314mol/L
B. 0��4 min��ƽ����Ӧ����v(H2O2)��3.75��10-2mol/(L��min)
C. 6��10 min�����������ƽ����Ӧ����v(H2O2)��2.75��10-2mol/(L��min)
D. ��Ӧ��6 minʱ��H2O2�ֽ���50%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��X(g)+2Y(g)![]()
![]() 2Z(g) ����2M��g��
2Z(g) ����2M��g��![]() N��g��+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼʾ��
N��g��+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼʾ��
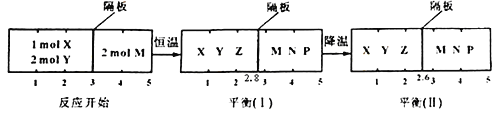
�����ж���ȷ����
A. ��Ӧ�ٵ�����Ӧ�����ȷ�Ӧ
B. ��ƽ�⣨I��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
C. ��ƽ�⣨I��ʱ��X��ת����Ϊ![]()
D. ��ƽ�⣨I����ƽ�⣨II����M������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10 mL 0.1 mol��L��1��HR��Һ����ε���0.1 mol��L��1��NH3��H2O��Һ��������ҺpH�������Ա仯��ͼ�����з�����ȷ����

A. b��c��Һ����������Ũ�ȶ���С
B. b����ҺpH��7��˵��NH4Rû��ˮ��
C. c����Һ�д���c(R��) > c(NH4+)��c(H��)> c(OH��)
D. a��b����������ǿ��˵��HRΪ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���Ͽ�������ṩ����ࡢ���ۡ���������ˮ�磬�൱��ÿ��ȼ��3000���ԭú�Ļ������糧�����ĵ��ܣ������Ͽ���������ڿ���
������ЧӦ ��S02���ŷ� �۰�ɫ��Ⱦ �ܳ����ն�
A. �٢ڢۢ� B. �٢ڢ� C. �٢ڢ� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH4��NH3��H2O��HF�ǵڶ����ڵ��⻯�Ҳ�����������е���Ҫ���ʡ�
(1)��25 ����101 kPaʱ��16 g CH4��ȫȼ������Һ̬ˮʱ�ų���������890.31 kJ����CH4��ȼ����Ϊ________________��
(2) NH3��H2O���ȶ��Խϸߵ���:___________��NH3��PH3�зе�ϸߵ���:__________��
(3)��ͼ��ʾ��ɱպϻ�·�����У���װ������CH4��O2��CO2Ϊ��Ӧ�ϡ����������Ϊ�缫��������̼����Ϊ������γɵ�ԭ��أ���װ����a��bΪʯī��b�����к�ɫ����������CuSO4��Һ�����Ϊ200 mL��

��װ��������AΪ________(����CH4������O2��CO2��)��d���ϵĵ缫��ӦʽΪ_______________________________________��
����װ����a���ϵĵ缫��ӦʽΪ___________________��
����a������112 mL(��״��)���壬���װ��������CH4________mL(��״��)����װ����������Һ��pH��________(���Ե��ǰ����Һ����仯)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(H2NNH2)��һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯����ͼ��ʾ����֪����1 mol��ѧ�����������(kJ)��N��NΪ942��O=OΪ500��N��NΪ154�������1 mol N��H�����������(kJ)�ǣ�

A. 194 B. 391 C. 516 D. 658
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com