
【题目】有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧聚乙炔.其中既能使酸性KMnO4溶液褪色,也能与溴水反应而使溴水褪色的是( )
A.②③⑤
B.②③⑦
C.②③⑧
D.②③⑦⑧
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Na2CO3、NaHCO3的性质.回答下列问题:
(1)甲组同学分别取1.0g Na2CO3、NaHCO3固体,各滴加几滴水,发现盛Na2CO3的试管温度上升,而盛NaHCO3的试管温度下降;原因是 .
(2)乙组同学分别取0.1mol/L Na2CO3、0.1mol/LNaHCO3的溶液,用0.1mol/LHCl溶液滴定,pH变化与盐酸体积的关系如图所示: 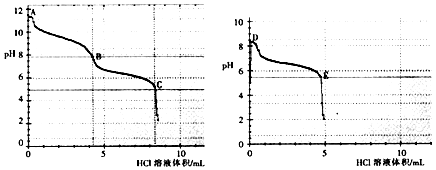
①碳酸钠与盐酸反应pH有两次突变,达到两次反应终点,分别是(填A、B、C、D或E).
②B点的主要溶质是(用化学式表示).
③B点(填“大于”或“小于”) D点的pH,主要原因是 .
(3)丙组同学预测NaHCO3有酸性,向其溶液加入镁粉,发现有气泡和沉淀生成,写出化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项操作中,错误的是
A.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
B.进行分液时,分液漏斗中的下层液体从下口流出,上层液体从上口倒出
C.萃取分液前需对分液漏斗检漏
D.为保证分流漏斗内的液体顺利流出,需将上面的塞子拿下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的摩尔体积比乙的摩尔体积小
C.甲的相对分子质量比乙的相对分子质量小
D.甲的物质的量比乙的物质的量少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 碱性:LiOH>NaOH>KOH>RbOH
B. 金属性:Rb>K>Na>Li
C. 和酸反应时Fe能失2e-,Na失e-,所以Fe的金属性强于Na
D. Rb不易与水反应放出H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于碱金属元素的表述正确的是( )
A. 碱金属是同周期中金属性最强的元素B. 从上至下单质金属性逐渐减弱
C. Li、Na、K单质均应保存在煤油中D. Li、Na、K燃烧均生成过氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化剂和还原剂在生产生活中广泛使用.已知高锰酸钾和浓盐酸可以发生如下反应:
2KMnO4+16HCl=5Cl2↑+2MnCl2+2KCl+8H2O
(1)在该反应中还原剂为 , 还原产物为
(2)用双线桥表示该反应中电子转移的方向和数目2KMnO4+16HCl=5Cl2↑+2MnCl2+2KCl+8H2O
(3)若有0.8mol还原剂被氧化,则转移电子的物质的量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家规定,酿造食醋的总酸含量标准为3.5~5.0g/100mL(总酸含量即100mL食醋中CH3COOH的质量).某化学兴趣小组为测定某市售食醋的总酸含量,进行了实验.实验后,得知10.0mL该食醋样品与7.5g溶质的质量分数为4%的氢氧化钠溶液恰好完全反应.计算该市售食醋样品中的总酸含量,并说明是否符合国家标准.(假设该市售食醋样品中其他物质不与氢氧化钠发生反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下: 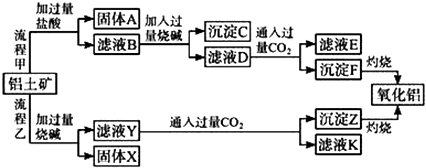
请回答下列问题:
(1)滤液Y中通入过量CO2的离子方程式为、 .
(2)验证滤液B含Fe3+ , 可取少量滤液并加入(填试剂名称).
(3)列举氧化铝的工业用途之一 .
(4)指出流程乙的一个缺点是 .
(5)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X.已知每转移6.02×1023个电子,有0.5mol化合物X生成,此反应的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com