
【题目】下列实验或操作方法正确的是

A.实验Ⅰ:干燥并收集 NH3
B.实验Ⅱ:制作红色喷泉
C.实验Ⅲ:制取乙酸乙酯
D.实验Ⅳ:分离苯和甲苯
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是( )
A.向硫酸铁溶液中加入过量铁粉:Fe+2Fe3+=3Fe2+
B.向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+=2Na++CO2↑+H2O
C.向铜粉中加入稀硫酸:Cu+2H+=Cu2++H2↑
D.向铝粉中加入足量NaOH溶液:2Al+2OH-=2AlO![]() +H2↑
+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L恒容密闭容器中投入一定量的A、B发生反应:3A(g)+bB(g)![]() cC(g) H=-QkJ·mol-1(Q>0),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是
cC(g) H=-QkJ·mol-1(Q>0),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是
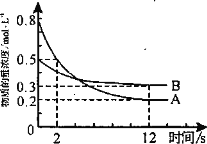
A. 2s时,A的反应速率为0.15mol·L-1·s-1
B. 图中交点时A的消耗速率等于A的生成速率
C. 化学计量数之比b ∶c = 1∶2
D. 12s内反应放出0.2QkJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:
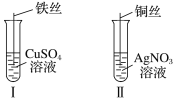
①Ⅰ中发生反应的离子方程式为__________________________________;
②Ⅱ中铜丝上观察到的现象是___________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中氧化产物是________
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______(填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为________________________________________________
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某黄色溶液中可能含有Na+、NH4+、Fe2+、Fe3+、Cl﹣、SO42﹣、CO32﹣等离子(不考虑水的电离和离子的水解)。某同学为了确定其组分,设计并完成了如下实验:

下列说法正确的是( )
A.c(Fe3+)一定为0.2 molL﹣1
B.c(Cl﹣)至少为0.2 molL﹣1
C.Na+'、SO42﹣一定存在,NH4+一定不存在
D.Na+、Fe2+可能存在,CO32﹣一定不存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若某原子在处于能量最低状态时,外围电子排布为![]() ,则下列说法错误的是
,则下列说法错误的是
A. 该元素可能有+3价
B. 该元素位于第5周期副族
C. 该元素原子核外共有39个不同运动状态的电子
D. 该元素基态原子第N能层上还有5个空轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列结构示意图,判断下列说法中正确的是

A. 在NaCl晶体中,距Na+最近的多个Cl-构成正四面体
B. 在CaF2晶体中,Ca2+的配位数为4
C. 在金刚石晶体中,碳原子与碳碳键数之比为1:2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)是一种片层状结构的白色晶体(下图),有油腻感,可做润滑剂。硼酸对人体受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。回答下列问题:
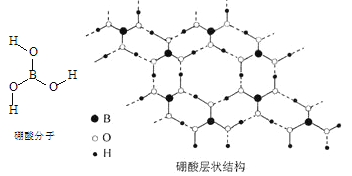
(1)B原子的结构示意图为_____________________;
(2)硼酸为一元弱酸,在水中电离方程式为H3BO3+H2O![]() [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_________________________;
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_________________________;
(3)下列有关硼酸晶体的说法正确的是__________;
A.H3BO3分子的稳定性与氢键有关
B.含1 molH3BO3的晶体中有3 mol氢键
C.分子中B、O最外层均为8e-稳定结构
D.B原子杂化轨道的类型sp2,同层分子间的主要作用力是范德华力
(4)根据对角线规则,与B性质相似的元素是__________。
(5)含氧酸的通式为(HO)mROn,根据非羟基氧原子数判断,与H3BO3酸性最接近的是________;
A.HClO B.H4SiO4 C.H3PO4 D.HNO2
(6)一种硼酸盐的阴离子为B3O6n-,n=_____________;B3O6n-结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O6n-的结构图(注明所带电荷数); _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向氨水中加入盐酸至中性,溶液中![]() <1
<1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com