
【题目】氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:
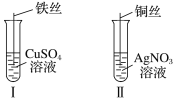
①Ⅰ中发生反应的离子方程式为__________________________________;
②Ⅱ中铜丝上观察到的现象是___________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中氧化产物是________
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______(填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为________________________________________________
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。________________________________________________
【答案】Fe+Cu2+=Fe2++Cu 红色铜丝上有银白色金属附着,无色溶液变为蓝色 Ag+>Cu2+>Fe2+ CO2 还原性 Fe+2HCl=FeCl2+H2↑ 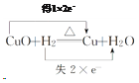
【解析】
(1)①Fe丝与CuSO4溶液反应的离子方程式为:Fe+Cu2+=Fe2++Cu,故答案为:Fe+Cu2+=Fe2++Cu;
②铜丝和AgNO3溶液反应生成Ag和Cu(NO3)2,现象为:红色铜丝上有银白色金属附着,无色溶液变为蓝色,故答案为:红色铜丝上有银白色金属附着,无色溶液变为蓝色;
③Fe置换出Cu,说明Fe比Cu活泼,而氧化性:Cu2+>Fe2+,Cu置换出Ag,说明Cu比Ag活泼,而氧化性:Ag+>Cu2+,综上所述,氧化性:Ag+>Cu2+>Fe2+,故答案为:Ag+>Cu2+>Fe2+;
(2)2KNO3+3C+S=K2S+N2↑+3CO2↑中C化合价升高,被氧化成CO2,CO2是氧化产物,故答案为:CO2;
(3)服用维生素C,可使Fe3+转化成Fe2+,使Fe元素的化合价降低,将Fe3+还原为Fe2+,说明维生素C具有还原性,故答案为:还原性;
(4)铁与盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑,故答案为:Fe+2HCl=FeCl2+H2↑;
(5)氢气和氧化铜在加热条件下反应生成铜和水,反应的方程式为:CuO+H2![]() Cu+H2O,用双线桥表示电子转移的方向和数目如下:
Cu+H2O,用双线桥表示电子转移的方向和数目如下: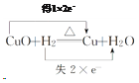 ,故答案为:
,故答案为: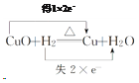 。
。


科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列叙述错误的是( )
A. 18g H2O中含的质子数为10NA
B. 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
C. 46g NO2和N2O4混合气体中含有原子总数为3NA
D. 12g金刚石含有的共价键数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尼龙材料是一种性能优良的工程塑料,目前广泛应用于汽车领域,具有优异的力学性能。以A(C6H10)原料通过氧化反应制备G,再通过缩聚反应合成尼龙,合成路线如下:

回答下列问题:
(1)A的化学名称为_________________;
(2)B到C的反应类型为_______________;
(3)D中含有的官能团名称是____________;
(4)E的分子式为_____________;
(5)由G合成尼龙的化学方程式为________________________________;
(6)写出一种与C互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积之比为3:1)_____________。
(7)1,4-二溴环己烯(![]() )是多数有机合成一种重要的中间体,设计由B为起始原料制备1,4-二溴环己烯的合成路线____________________。
)是多数有机合成一种重要的中间体,设计由B为起始原料制备1,4-二溴环己烯的合成路线____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物J是我国自主成功研发的一种新药。合成J的一种路线如图:
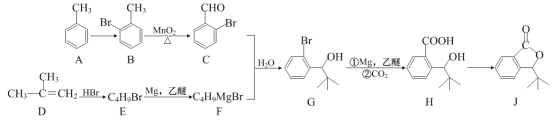
(1)由A生成B的反应所需的试剂及反应条件为___。
(2)由B生成C的反应类型为___。
(3)D___(填写“存在”或“不存在”)顺反异构现象。
(4)C与新制氢氧化铜反应的化学方程式为___(该条件下苯环上的溴不参与反应)。
(5)写出同时满足下列条件的J的一种同分异构体的结构简式___。
①分子中除苯环外不含其它环状结构;
②能发生银镜反应;
③分子中只含有有2种不同化学环境的氢。
(6)写出以乙醇和乙酸为原料制备![]() 的合成路线图___(无机试剂和乙醚任用,合成路线图示例见本题题干)。
的合成路线图___(无机试剂和乙醚任用,合成路线图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀),下列分析正确的是
![]()
A. 用98%的浓硫酸配制4.5 mol·L—1稀硫酸,只需3种玻璃仪器
B. 步骤②目的是将溶液Ⅰ中的Fe2+氧化成Fe3+,操作是通入足量的氯气
C. 用Cu(OH)2 替代CuO也可调节溶液pH而不影响实验结果
D. 操作⑤是蒸发结晶,所需仪器是蒸发皿、玻璃棒、酒精灯、泥三角、三脚架
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15 分)化合物H 是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
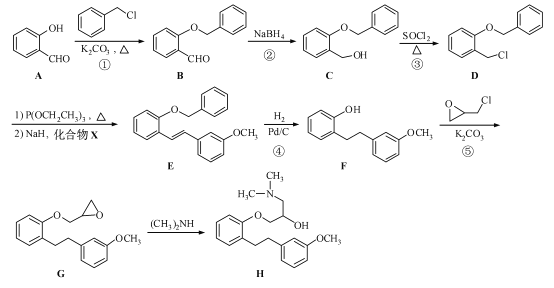
(1)化合物A 中的含氧官能团为 和 (填官能团名称)。
(2)反应①→⑤中,属于取代反应的是 (填序号)。
(3)写出同时满足下列条件的B 的一种同分异构体的结构简式: 。
I. 分子中含有两个苯环;II. 分子中有7 种不同化学环境的氢;III. 不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
(4)实现D→E 的转化中,加入的化合物X 能发生银镜反应,X 的结构简式为 。
(5)已知:![]() 。化合物
。化合物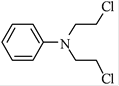 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以![]() 和
和![]() 为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一容积为 2L 的恒容密闭容器中,A、B、C、D 四种气体物质发生可逆反应,其物质的量 n(mol)随时间 t(min)的变化曲线如图所示。回答下列问题:
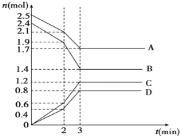
(1)该反应的化学方程式为____。
(2)前 2min 内用 A 的浓度变化表示的化学反应速率为____;
(3)在 2min 时,图象发生改变的原因可能是_____ (填字母)
A.增大 B 的物质的量 B.降低温度 C.加入催化剂 D.减小 A 的物质的量
(4)不同条件下的该反应的速率:①v(A)=1.0mol·L-1·s-1,②v(B)=1.0 m ol·L-1·s-1,③v(C)=1.2 mol·L-1·s-1,④v(D)=1.2mol·L-1·s-1。其中反应速率最快的是___ (填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国学者研制了一种纳米反应器,用于催化草酸二甲酯(DMO)和氢气反应获得EG。反应过程示意图如下:
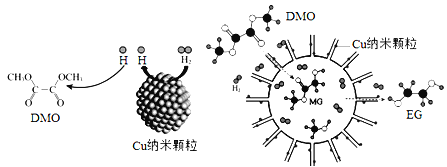
下列说法不正确的是
A. Cu纳米颗粒将氢气解离成氢原子
B. 1mol DMO分子进行水解可以得到1mol甲醇
C. 反应过程中生成了MG和甲醇
D. EG和甲醇不是同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com