
【题目】下列生活、生产的运用中涉及了氧化还原反应的是
A. 用Al(OH)3治疗胃酸过多 B. 用熟石灰中和土壤的酸性
C. 用金属铝进行铝热法炼铁 D. 用水玻璃制备硅胶和木材防火剂
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. SO32-中硫原子的杂化方式为sp2 B. C2H2分子中含有3个σ键和2个π键
C. H2O分子中氧原子的杂化方式为sp2 D. BF3分子空间构型呈三角锥形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知丙酮(C3H6O)通常是无色液体,易溶于水,密度小于1 g·mL-1,沸点约为55℃。要从水与丙酮的混合物中将丙酮分离出来,下列方法中最为合理的是( )
A.蒸馏 B.分液 C.过滤 D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,由相同种类元素组成的是( )
A. 胆固醇、脂肪酸、脂肪酶 B. 淀粉、核糖、糖原
C. 氨基酸、核苷酸、丙酮酸 D. 性激素、生长激素、胰岛素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
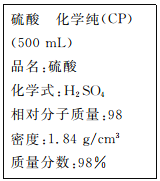
(1)该硫酸的物质的量浓度为____________mol/L。
(2)某化学小组进行硫酸酸性实验探究时,需要240 ml,4.6 mol.L-l的稀硫酸,则在配制时需要取上述浓硫酸_____________mL。
(3)叙述将上述浓硫酸进行稀释的实验操作:____________________。
(4)在配制4.6 mol.L-l稀硫酸的过程中,下列情况对所配制的硫酸溶液的物质的量浓度有何影响?
①用量筒量取浓硫酸时俯视量筒刻度线_____________(填“偏高”、“偏低”或“无影响”,下同);
②未经冷却趁热将溶液注入容量瓶中:_____________;
③仰视容量瓶刻度线定容:__________________;
④移液时不慎将少量溶液滴在容量瓶外面:_____________;
(5)实验过程中出现下列情况应如何处理?
①向容量瓶中加入蒸馏水,液面离容量瓶颈刻度线下1~2 cm时,应_____________。
②加蒸馏水时不慎超过了容量瓶颈刻度线,应_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到测量要求的是( )
A. 用托盘天平称量25.21 g氯化钠
B. 用10 mL量筒量取7.50 mL稀硫酸
C. 用25 mL滴定管量取14.86 mL溶液
D. 用广泛pH试纸测得溶液的pH为4.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨对化学工业和国防工业具有重要意义。


(1)根据图1请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)
(2)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图2为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
①图2中氨气的体积分数为15%时,H2的转化率为 。
②图3中T=450℃,则温度为500℃时对应的曲线是 (填“a”或“b”)。
(3)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:

①分析表中数据,判断5 min时反应是否处于平衡状态? (填“是”或“否”),前5 min反应的平均反应速率v(CH4) = 。
②在相同实验条件下,若改为加入CH4 0.1mol,若要求平衡后H2在反应混合气中质量分数不变,则还需加入的物质及其物质的量为
③反应在7~10 min内,CO的物质的量减少的原因可能是 (填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④下列方法中可以证明上述已达平衡状态的是
a.单位时间内生成3n mol H2的同时生成n mol CO
b.容器内压强不再变化
c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化
e.CH4的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:

则反应CO(g)+H2O(g)![]() CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_________.
CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2+B2![]() 2AB ΔH=QkJ/mol。在不同温度和压强改变条件下,产物AB的生成情况如图所示:a为500℃,b为300℃时的情况,c为300℃时从时间t3开始向容器加压的情况,则下列叙述正确的是
2AB ΔH=QkJ/mol。在不同温度和压强改变条件下,产物AB的生成情况如图所示:a为500℃,b为300℃时的情况,c为300℃时从时间t3开始向容器加压的情况,则下列叙述正确的是

A.AB为气体,A2、B2中最少有一种为非气体,Q>0
B.AB为气体,A2、B2中最少有一种为非气体,Q<0
C.AB为固体,A2、B2中最少有一种为非气体,Q<0
D.A2、B2、AB均为气体,Q>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com