
| A. | ①或② | B. | ①或④ | C. | ②或③ | D. | ②或④ |
分析 若A为金属单质,A为+1价金属,则1mol单质A与浓硝酸反应生成1molNO2和1mol硝酸盐;A为+2价金属,则1mol单质A与浓硝酸反应生成2molNO2和1mol硝酸盐;
A为+3价金属,则1mol单质A与浓硝酸反应生成3molNO2和1mol硝酸盐;
若A为非金属单质,如单质碳,则1mol单质A与浓硝酸反应生成4molNO2,结合原子守恒分析.
解答 解:若A为金属单质,A为+1价金属,则1mol单质A与浓硝酸反应生成1molNO2和1mol硝酸盐,所以消耗的硝酸为2mol,与题意不符;
A为+2价金属,则1mol单质A与浓硝酸反应生成2molNO2和1molA(NO3)2,所以消耗的硝酸为4mol,与题意相符;
A为+3价金属,则1mol单质A与浓硝酸反应生成3molNO2和1molA(NO3)3,所以消耗的硝酸为6mol,与题意不符;
若A为非金属单质,如单质碳,则1mol单质A与浓硝酸反应生成4molNO2,反应消耗4mol硝酸,与题意相符;
综上可知组成单质A的元素在反应后的化合价可为+2或+4;
故选D.
点评 本题考查了有关硝酸的计算,题目难度中等,注意把握反应产物的判断结合原子守恒和得失电子守恒计算,侧重于考查学生的分析能力和计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |  | 白色结晶粉末 | 170~ 172℃ | 易溶 于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
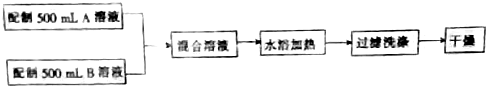
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
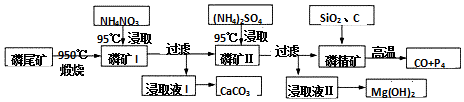
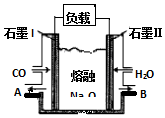
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
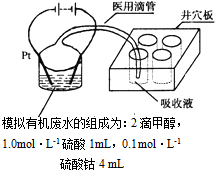 汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol•L-1 | B. | 1mol•L-1 | C. | 1.5mol•L-1 | D. | 2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )| A. | 常温下ka(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) | |
| B. | pH=13时,溶液中不存在HC03-的水解平衡 | |
| C. | pH由8~11时,$\frac{(C{O}_{3}^{2-})•c({H}^{+})}{c(HC{O}_{3}^{-})}$不变 | |
| D. | pH=3时,有c(NH4+)+c(NH3•H2O)═c(HCO3-)+c(CO32-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管、容量瓶和分液漏斗使用前都要检漏、干燥 | |
| B. | 滴定管没有用标准液润洗,会导致测定结果偏高 | |
| C. | 滴定管中加标准液后,要调节液面位置在零刻度或以下 | |
| D. | 胆矾结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com