
如下图所示为常见仪器的部分结构。
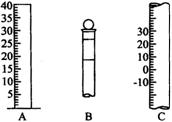
(1)请写出下列仪器的名称:A________,B________,C________。
(2)仪器B上标记有________(填序号)。
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
(3)检验仪器B是否漏水的方法是________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
设为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,15g甲基(-CH3)所含的中子数为6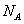
B.一定条件下足量的Fe粉与浓硫酸反应,转移电子数一定为3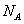
C.在1L的碳酸钠溶液中,若c(CO32-)=1mol/L,则Na+个数为2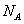
D.含4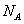 个离子的固体Na2O2溶于水配成1L溶液,所得溶液中Na+的浓度为1mol/L
个离子的固体Na2O2溶于水配成1L溶液,所得溶液中Na+的浓度为1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个
“封管实验”(夹持装置未画出),判断下列说法正确的是( )
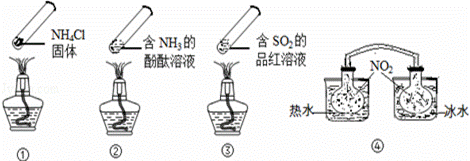
A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好
B.加热时,②、③溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内
气体颜色变浅
D.四个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.1 L水中溶解了40 g NaOH后,所得溶液浓度为1 mol/L
B.从1 L 2 mol/L的NaCl溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.将标准状况下的HCl气体2.24 L通入水中制成100 mL溶液,所得溶液的物质的量浓度为1 mol/L
D.配制1 L 0.2 mol/L的CuSO4溶液,需用25 g胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
某500mL溶液中含0.1 mol Fe2+.0.2molFe3+,加入0.2mol铁粉,待Fe3+ 完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变) ( )
(提示:2 Fe3+ + Fe =3 Fe2+ )
A.0.4 mol/L B.0.6 mol/L C.0.8 mol/L D. l.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.1 mol任何气体所占体积都约是22.4 L
B.1 mol H2O(g)在标准状况下体积为22.4 L
C.1 mol气体体积为22.4 L,则一定是标准状况
D.气体摩尔体积不一定是22.4 L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
300 mL某浓度的NaOH溶液中含有60 g溶质。现欲配制1 mol·L―1的NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
A.1∶4 B.1∶5 C.2∶1 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述违背化学原理的是( )
A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
D.饱和石灰水中加入少量CaO,恢复到原温度时,溶液中c(OH-)不变,OH-数目减少
查看答案和解析>>
科目:高中化学 来源: 题型:
无水氯化镁是制备某种催化剂的中间体。某研究性学习小组设计实验方案进行制取无水氯化镁等实验。请填写下列空白。
[实验一]利用下图实验装置(夹持和加热装置省略),在HCl气流中小心加热MgCl2·6H2O晶体制取无水氯化镁(无水氯化镁易吸水)。烧瓶中发生的反应为: NaCl+H2SO4(浓)== NaHSO4+HCl↑

 (1)试剂X是 。
(1)试剂X是 。
(2)该实验装置存在一个缺陷是  。
。
[实验二]通过下列步骤,测定实验一所得产物中氯元素含量以确定产物是否含有结晶水:
①称取m1g样品置于烧杯中,充分溶解;②加入足量硝酸银溶液, 充分反应后,过滤;③洗涤沉淀,干燥至恒重,称得沉淀质量为m2g。
充分反应后,过滤;③洗涤沉淀,干燥至恒重,称得沉淀质量为m2g。
(3)若步骤③的操作中未洗涤沉淀,将导致测得的氯元素含量 (填“偏高”或“偏低”)
(4)若测得m1=10.40,m2=28.70,则所得产品MgCl2·nH2O中n的值为 。
[实验三]一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化效果的影响,设计如下对比实验:
| 实验序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式 | 催化效果/g·g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 | ω | 100 | 振动球磨 | 6.5×104 |
注:催化效果用单位时间内每克催化剂得到产品的质量来表示
(5)表中ω= 。
(6)从实验1、2可以得出的结论是 。
(7)设计实验2、3的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com