
����Ŀ���о���ѧϰС�����������й�װ�ý���̽��ʵ�飬�ش�������⡣
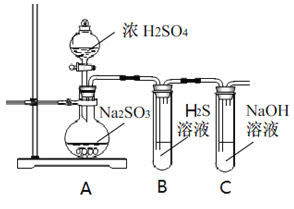

��1��д��A�еķ�Ӧ��ѧ����ʽ_______________________________________________________
��2��ʵ��ʱ������װ��A�з�Һ©��������������Һ����������������ֹͣ������ܵ�ԭ����_________________________________��
��3��װ��B�е���Һ���ֻ��ǣ���ʵ��֤��SO2����___�� ��
��4��ʵ��ⶨװ��C����Һ�ʼ��ԡ���ҺΪʲô�ʼ����أ�����в�ͬ������������ɵ�Na2SO3ˮ�⣻������������ʣ�ࡣ�����ʵ�鷽��֤���������������ѡ�������Լ�����ʵ�飺Na2SO3��Һ����̪��Һ����ˮ��BaCl2��Һ��ϡ����
ʵ�鲽�� | ʵ����� | Ԥ����������� |
_____ | _______________ | _______________ |
��5����һС������װ��D����ʵ�飺��ע������װ��D��ע��v mLʵ�����Ʊ�SO2�Ŀ���������Һ�պ���ɫ��ֹͣʵ�顣��С���ʵ��Ŀ����_________________________________��
���𰸡� Na2SO3������+H2SO4��Ũ���� Na2SO4 + SO2��+ H2O û�д�Һ©�����Ͽڻ��������Һ©���Ͽڻ����ϵİ���û�����Һ©���ϵ�С����ͨ��������������������ͨ ������ I ȡ������Һ���Թ������뼸�η�̪��Ȼ�����������BaCl2��Һ ��Һ�ȱ����Ȼ������������������ɫ��ȥ����˵������ȷ������ɫ������ȥ����˵������ȷ �ⶨʵ���ҿ�����SO2����
�������������������1��A��ŨH2SO4��Na2SO3��Ӧ����SO2�����Ի�ѧ����ʽΪ��Na2SO3���̣�+H2SO4��Ũ���� Na2SO4 + SO2��+ H2O��
��2�����û�д�Һ©�����Ͽڻ��������Һ©���Ͽڻ����ϵİ���û�����Һ©���ϵ�С����ͨ����Ũ������������ʱ����Һ©��Ϊ�ܱ�������Ũ���������С���������������ѹǿ��С���ᵼ��Һ����������������ֹͣ��
��3��װ��B�е���Һ���ֻ��ǣ�SO2��H2S��Ӧ����S������H2O��SO2��SԪ�ػ��ϼ۽��ͣ����Ը�ʵ��֤��SO2���������ԡ�
��4����������ɵ�Na2SO3ˮ��ʹ��Һ�ʼ��ԣ�����������BaCl2��Һ��Na2SO3��BaCl2��Ӧ����BaSO3������Na2SO3��ˮ��ƽ�������ƶ�����Һ��ɫ��ȥ��������������ʣ�ർ����Һ�ʼ��ԣ���������BaCl2��Һ����Һ��Ȼ�ʼ��ԣ���ɫ������ȥ��
��5������Һ�պ���ɫ��ֹͣʵ�飬��ͨ��ע������������ʣ����������������ͨ����ʵ��ɲⶨʵ���ҿ�����SO2������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ý���ʵ�飬���ж�ʵ������Ľ��Ͳ���������
ѡ�� | �����Լ� | �������� | ���� |
|
A | Ʒ����Һ | ��Һ��ɫ | SO2����Ư���� | |
B | Na2SiO3��Һ | ������״���� | ���ԣ�H2SO3>H2SiO3 | |
C | ����KMnO4��Һ | ��ɫ��ȥ | SO2���л�ԭ�� | |
D | Ba(NO3)2��Һ | ���ɰ�ɫ���� | SO32-��Ba2+���ɰ�ɫBaSO3���� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺
��1��������ˮ�����������»�����������ɫ����Ϊ_______(�ѧʽ)��
��2����������ò����Լ�ƿʢװ����������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______��
��3��ʵ���ҳ���Al2(SO4)3��NH3��H2O�Ʊ�Al(OH)3�䷴Ӧ�����ӷ���ʽΪ_______��
��4���ò�����պŨ������ڻ���ϣ����ڣ�Ũ������ֳ���������Ϊ_______��
��5��ά����C�ܽ�������ȡ��Fe3+ת��ΪFe2+,˵��ά����C����_______(ѡ������������������ԭ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������������ԭ��Ӧ����
A. Fe��CuSO4===FeSO4��Cu B. NH4HCO3![]() NH3����H2O��CO2��
NH3����H2O��CO2��
C. Cl2��H2O![]() HCl��HClO D. Fe2O3��3CO
HCl��HClO D. Fe2O3��3CO![]() 2Fe��3CO2
2Fe��3CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͭ�Ƚ������仯�������ճ�������Ӧ�ù㷺����ش��������⣺
��1���������������壮������FeS2�������������ұ����������Ҫԭ�ϣ�����һ����ӦΪ3FeS2+8O2 ![]() 6SO2+Fe3O4 �� ��������Ϊ �� ����3molFeS2�μӷ�Ӧ��ת��mol���ӣ�
6SO2+Fe3O4 �� ��������Ϊ �� ����3molFeS2�μӷ�Ӧ��ת��mol���ӣ�
��2�����ļ۵����Ų�ʽΪ �� ����������ˮ������ԭ��Ϊ�������ӷ���ʽ��ʾ����
��3������Cu�����백ˮ����˫��ˮ������Ӧ����������ߵĻ����Һ��Ӧ��������ɫ��Һ��Cu�백ˮ��˫��ˮ��Ӧ�����ӷ���ʽ��
��4��������һ�ֺ�ɫ���ϣ���ɷ���Fe2O3 �� ��һ��������������160mL5molL��1�����У��ټ���һ��������ǡ���ܽ⣬�ռ���2.24L��������״�������������Һ����Fe3+ �� �μӷ�Ӧ�����۵�����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3mol��Ȳ��5mol�������ܱ������з�Ӧ������ﵽƽ��ʱ������amol��ϩ����ƽ����������ȫȼ������CO2��H2O���������������ʵ����ǣ�������
A.6mol
B.10mol
C.3amol
D.3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ���������ʱ�����ü���ŨH2SO4���ǣ�������
A.�ɱ���ȡ������
B.��������Ҵ��Ʊ���������
C.������������ϩ
D.���Ҵ�����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ����ѧϰС���ͬѧ���ʵ����֤���ڶ�����̼��ȼ�յIJ���ش��������⣺
(1)����ͬѧ��������װ�D��ȡ���﴿���Ķ�����̼������X��������________________��װ��B��ʢװ���Լ���_________________��

(2)����ͬѧ���ü����Ƶõ�CO2��ѡ������װ��(���ظ�ʹ��)��֤���ڶ�����̼��ȼ�յIJ������Ƿ���CO��

��F��ʢװ���Լ���__________________��
��װ����ȷ������˳��ΪC��_______��______��______��E��_______��_______H��
��֤��ȼ�յIJ����к���CO��������_______________��
(3)����ͬѧȡ����ͬѧ��Gװ�������õĹ������Թ��У���������ϡ���ᣬ������������Թܵײ��к�ɫ���������������һ����__________________(�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����(�� ��)
A. ̼��������Һ����������ʯ��ˮ��Ӧ��HC![]() +Ca2++OH��CaCO3��+H2O
+Ca2++OH��CaCO3��+H2O
B. �Ȼ������������������Һ��ϼ��ȣ�N![]() +OH��
+OH��![]() H2O+NH3��
H2O+NH3��
C. �ƺ���ˮ��Ӧ��Na��2H2ONa+��2OH����H2��
D. ���Ȼ�����Һ�еμӹ�����ˮ��Al3++3OH��Al(OH)3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com