
硅、铝和铁及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)30Si原子的中子数为 ,Si的晶体类型为 。
(3)Al3+与Yn—的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是 。
(4)某焊药熔渣36.0g(含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,分离得到11.0g固体,滤液中加入过量NaOH溶液,分离得到21.4g固体。则此熔渣中Al2O3的质量分数为
。
(1)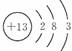 ,2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑
,2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑
(2) 16 原子晶体 (3) HCl (4)25%
解析试题分析:(1)Al是13号元素,所以Al的原子结构示意图为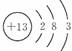 ;Al与NaOH溶液反应的离子方程式为2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑。
;Al与NaOH溶液反应的离子方程式为2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑。
(2)中子数和质子数之和是质量数,30Si原子的中子数为30-14=16。Si的结构与金刚石相似,所以晶体类型为原子晶体。
(3)Al3+与Yn—的电子数相同,所以Y是第二周期的元素。Y所在族各元素的氢化物的水溶液均显酸性,所以是第ⅦA族元素。由于HF分子间存在氢键,所以该族氢化物中沸点最低的是HCl。
(4)二氧化硅与盐酸不反应,所以11.0g固体是二氧化硅。氢氧化铝是两性氢氧化物,能溶解再氢氧化钠溶液中,因此得到的21.4g固体是氢氧化铁,物质的量是0.2mol没声音根据铁原子守恒可知,氧化铁的物质的量是0.1mol,质量是16g,则氧化铝的质量是36.0g-16g-11.0g=9g,因此氧化铝的质量分数是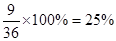 。
。
考点:考查原子结构示意图、方程式、晶体类型以及物质含量的测定
点评:固体是高考中的常见题型,属于基础性试题的考查,难度不大。主要是对学生基础性知识的巩固与检验,同时兼顾对学生能力的培养,有利于培养学生的应试能力,提高学生灵活运用基础知识解决实际问题的能力。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年福建省龙岩市高三上学期期末考试化学试卷(解析版) 题型:填空题
铁、铝、铜及其化合物在生产、生活中有广泛的用途,试回答下列问题:
(1)铝的原子结构示意图为___________;铁、铝、铜三种金属的金属活动性由弱到强的排列顺序是__________。
(2)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,请写出该反应的离子方程式:_________________。
(3)如图装置中,铁作________极,铜电极的电极反应式为_________________________。

(4)已知铜与稀硫酸不反应,但铜片在稀硫酸中长时间加热时溶液会呈蓝色,请用化学方程式表示其原因:__________________________________________________________。
(5)氯化铝广泛用作有机合成和石油工业的催化剂。将铝土矿粉(主要成分为A12O3)与焦炭混合后加热并通人氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式:_____________________________ ,该反应的氧化剂是_________________。
(6)某校兴趣小组为测定一种铁铝硅合金 (FexAlySiz) 粉末的组成,提出如下方案:准确称取1.46 g该合金粉末,加入过量盐酸溶液,充分反应后过滤,测定剩余固体质量0.07 g。向滤液中滴加足量NaOH浓溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧,得红棕色粉末1.60g,通过计算确定此合金的组成为________________ (填化学式)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
硅、铝和铁及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)30Si原子的中子数为 ,Si的晶体类型为 。
(3)Al3+与Yn—的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是 。
(4)某焊药熔渣36.0g(含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,分离得到11.0g固体,滤液中加入过量NaOH溶液,分离得到21.4g固体。则此熔渣中Al2O3的质量分数为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com