
【题目】乙醇和乙酸是生活中两种常见的有机物.下列说法正确的是( )
A.乙醇、乙酸都能与金属钠反应
B.乙醇、乙酸都能与NaOH溶液反应
C.乙醇、乙酸都能使紫色石蕊试液变红色
D.乙醇、乙酸互为同分异构体
科目:高中化学 来源: 题型:
【题目】常温向20mL 0.1mol·L-1氨水中滴加0.1mol·L-1盐酸,溶液pH随滴加盐酸溶液体积的变化如图2所示。下列说法正确的是

A. a点时,c(NH3·H2O)>c(C1-)>c(NH4+)>c(OH-)>c(H+)
B. a~b区域内c(NH4+)+c(NH3·H2O)=0.1mol·L-1
C. 当V(HC1)=10mL时,c(NH4+)-c(NH3·H2O)=2[c(OH-)-c(H+)]
D. 当V(HCl)=20mL时,c(H+)+c(C1-)>c(NH4+)+c(NH3·H2O)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向2L恒容密闭容器中充入1.0mol A和1.0mol B,反应A(g)+B(g)C(g)经过一段时间后达到平衡.反应过程中测定的部分数据见下表,下列说法正确的是( )
t/s | 0 | 5 | 15 | 25 | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5s的平均速率v(A)=0.17molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41molL﹣1 , 则反应的△H>0
C.相同温度下,起始时向容器中充入2.0mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20mol A,0.20mol B和1.0mol C,反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理废水中的CN-可用电解方法除去,其装置如图所示。已知电解时控制溶液pH为9~10并加入食盐,阳极产生的ClO-将CN-氧化为两种无污染的气体。下列说法不正确的是

A. 不能用铁作阳极材料
B. 加入食盐的目的是在阳极产生ClO-
C. 阴极的电极反应式为2H2O+2e-=H2↑+2OH-
D. 除去CN-的反应为2CN-+5C1O-+2H+=N2↑+2CO2↑+5Cl-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究铁、铜及其化合物的性质,某同学设计并进行了下列两组实验。
实验一:
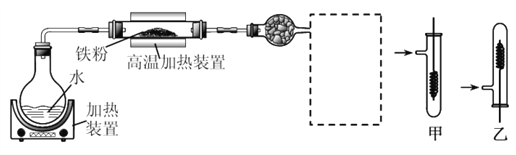
已知:3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
(1)虚线框处宜选择的装置是________(填“甲”或“乙”);实验时应先将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净氢气中,观察到的实验现象是______________________。
(2)实验后,为检验硬质玻璃管中的固体是否含+3价的铁元素,该同学取一定量的固体并用一定浓度的盐酸溶解,滴加_______溶液(填试剂名称或化学式),没有出现血红色,说明该固体中没有+3价的铁元素。请你判断该同学的结论是否正确并说明理由_________________。
实验二:
绿矾是含有一定量结晶水的硫酸亚铁,为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A 称重,记为m2 g,B为干燥管。按下图连接好装置进行实验。
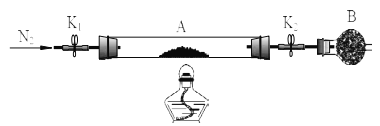
实验步骤如下:(1)________,(2)点燃酒精灯,加热,(3)______,(4)______,(5)______,
(6)称量A, 重复上述操作步骤,直至 A 恒重,记为m3 g。
(3)请将下列实验步骤的编号填写在对应步骤的横线上
a.关闭 K1 和 K2 b.熄灭酒精灯 c.打开 K1 和 K2 缓缓通入 N2 d.冷却至室温
(4)必须要进行恒重操作的原因是_________________。
(5)已知在上述实验条件下,绿矾受热只是失去结晶水,硫酸亚铁本身不会分解, 根据实验记录,
计算绿矾化学式中结晶水数目 x=__________________(用含 m1、 m2、 m3的列式表示)。
【答案】 乙 铜丝由黑变红 硫氰化钾或 KSCN 不正确,因为铁过量时: Fe+2Fe3+→3Fe2+ c b d a 确保绿矾中的结晶水已全部失去 ![]()
【解析】试题分析:实验一:(1)铁与水蒸气反应生成Fe3O4和氢气,虚线框中的装置是用氢气还原氧化铜的装置,根据氢气的密度比空气小分析;氧化铜被氢气还原为铜单质;(2)Fe3+能使KSCN溶液变成血红色;单质铁能把Fe3+还原为Fe2+;
实验二:(3)由于装置中含有空气,空气能氧化硫酸亚铁,所以加热前要排尽装置中的空气,利用氮气排出空气,为使生成的水蒸气完全排出,应该先熄灭酒精灯再关闭K1 和 K2;冷却后再称量;(4)进行恒重操作可以确保绿矾中的结晶水已全部失去;(5)根据题意,生成硫酸亚铁是![]() ,生成水的质量是
,生成水的质量是![]() ,根据
,根据![]() 计算x值;
计算x值;
解析:实验一:(1)铁与水蒸气反应生成Fe3O4和氢气,虚线框中的装置是用氢气还原氧化铜的装置,氢气的密度比空气小,所以用向下排空气法收集氢气,故选乙;氧化铜被氢气还原为铜单质,现象是铜丝由黑变红;(2)Fe3+能使KSCN溶液变成血红色,滴加KSCN溶液检验是否含有Fe3+,若溶液变为血红色,则含有Fe3+;单质铁能把Fe3+还原为Fe2+,当铁过量时: Fe+2Fe3+=3Fe2+,所以没有出现血红色,不能说明该固体中没有+3价的铁元素;
实验二:(3)由于装置中含有空气,空气能氧化硫酸亚铁,所以加热前要排尽装置中的空气,利用氮气排出空气,为使生成的水蒸气完全排出,应该先熄灭酒精灯再关闭K1 和 K2;冷却后再称量,正确的步骤是(1)打开 K1 和 K2 缓缓通入 N2,(2)点燃酒精灯,加热,(3)熄灭酒精灯,(4)冷却至室温,(5)关闭 K1 和 K2,(6)称量A, 重复上述操作步骤,直至 A 恒重,记为m3 g;(4)进行恒重操作可以确保绿矾中的结晶水已全部失去;(5根据题意,生成硫酸亚铁是![]() ,生成水的质量是
,生成水的质量是![]() ,
,
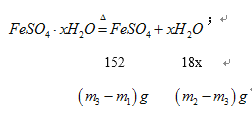
X=![]() 。
。
【题型】实验题
【结束】
24
【题目】PTT 是一种高分子材料,具有优异性能,能作为工程塑料、纺织纤维和地毯等材料而得到广泛应用。其合成路线可设计为:
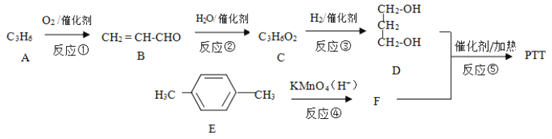
已知: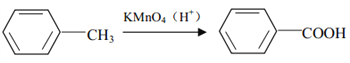
(1)B 中所含官能团的名称为_________,反应②的反应类型为_________。
(2)反应③的化学方程式为_________。
(3)写出 PTT 的结构简式_________。
(4)某有机物X 的分子式为C4H6O,X与B互为同系物,写出X可能的结构简式_________。
(5)请写出以 CH2=CH2 为主要原料(无机试剂任用)制备乙酸乙酯的合成路线流程图(须注明反应条件)。(合成路线常用的表示方式为:![]() )____________
)____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液的叙述中不正确的是
A. 等pH的盐酸与醋酸稀释后pH的变化如下图所示,则曲线II表示的是醋酸的稀释图象

B. 溶有等物质的量的NaCN、NaHCO3的溶液中:c(HCN)+C(CN-)=c(HCO3-)+c(H2CO3)+c(CO32-)
C. 25℃时,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa的溶溶液体积液等体积混合后pH=4:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)
D. 已知某温度下Ksp(CH3COOAg)=2.8×10-3,浓度均为0.1 mol·L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软质隐形眼镜材料W、树脂X的合成路线如图所示. 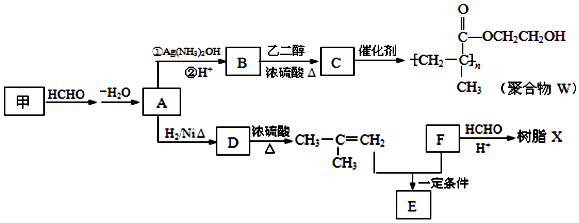
已知: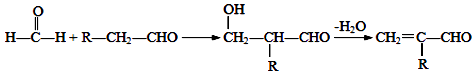
(1)A中含有的官能团的结构简式是 .
(2)甲的结构简式是 .
(3)B→C反应的化学方程式是 .
(4)B有多种同分异构体.属于酯且含有碳碳双键的同分异构体共有种(不考虑顺反异构.
(5)已知F的相对分子质量为110,1molF可与足量钠反应生成22.4L氢气(标准状况下),
苯环上的氢原子化学环境都相同.则F还能发生的反应是(填序号)
a.加成反应 b.氧化反应 c.加聚反应 d.水解反应
(6)写出树脂X可能的结构简式(写出一种即可).
(7)E的分子式为C10H14O2 , 含三个甲基,苯环上的一溴代物有两种,生成E的化学方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com