
目前,安全生产和食品、药品安全受到人们的高度重视。下列有关说法不正确的是
A.检查病人胃病所用的钡餐,只能用BaSO4,不可以用BaCO3
B.为了使馒头、银耳等洁白、卖相好,可以用点燃硫磺法熏蒸它们
C.可以用SO2来漂白纸浆、毛、丝、草帽辫等
D.“硫磺”温泉可以医治皮肤病
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案科目:高中化学 来源:2017届安徽省六安市高三上第一次月考化学试卷(解析版) 题型:选择题
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是
A.铁与氯气反应制氯化铁,推出铁与碘反应制碘化铁
B.CO2通入到漂白粉溶液中发生CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,
推出SO2通入到漂白粉溶液中发生SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO
C.Na2O2与CO2反应生成Na2CO3和O2,推出Na2O2与SO2反应可生成Na2SO3和O2
D.利用可溶性的铝盐溶液与氨水反应制Al(OH)3,推出可溶性的铁盐溶液与氨水反应制Fe(OH)3
查看答案和解析>>
科目:高中化学 来源:2017届河南省灵宝市高三上学期9月月考化学试卷(解析版) 题型:选择题
向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是( )
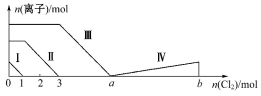
A.线段Ⅱ表示Br-的变化情况
B.原溶液中n(FeI2)∶n(FeBr2)=3∶1
C.根据图象无法计算a的值
D.线段Ⅳ表示IO3-的变化情况
查看答案和解析>>
科目:高中化学 来源:2017届河南省灵宝市高三上学期9月月考化学试卷(解析版) 题型:选择题
根据海水综合利用的工业流程图,判断下列说法正确的是
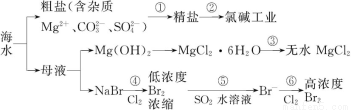
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2·6H2O在空气中灼烧即可制得无水MgCl2
C.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
D.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2.24 L Cl2
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:填空题
呼吸面具中Na2O2可吸收CO2放出O2,反应方程式为2Na2O2+2CO2 2Na2CO3+O2。若用超氧化钾(KO2)代替 Na2O2也可起到同样的作用。
2Na2CO3+O2。若用超氧化钾(KO2)代替 Na2O2也可起到同样的作用。
(1)写出KO2与CO2的反应方程式:______________。
(2)1 kg Na2O2和1 kg KO2分别和CO2反应,生成的O2体积比(同温同压下)为____________。
(3)等物质的量的CO2分别与足量Na2O2、KO2反应生成的O2体积比(同温同压下)为____________。
(4)你认为选用哪种物质作补氧剂更为合适?理由是什么?_______________________
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:填空题
含有下列离子的五种溶液①Ag+ ②Mg2+ ③Fe2+ ④Al3+ ⑤Fe3+试回答下列问题:
(1)既能被氧化又能被还原的离子是 (填离子符号,下同)
(2)向③中加入NaOH溶液,现象_________________,有关化学方程式为_____________________。
(3)加入过量NaOH溶液无沉淀的是________。
(4)加铁粉溶液质量增重的是________,溶液质量减轻的是________。
(5)遇KSCN溶液呈红色的是________。
(6)能用来鉴别Cl-存在的离子是________。
查看答案和解析>>
科目:高中化学 来源:2017届广东省等四校高三上学期第一次联考化学试卷(解析版) 题型:填空题
铁、钴(Co)、镍(Ni)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用.
(1)草酸钴(CoC₂O?)是一种难溶于水的浅粉红色粉末,通常用硫酸钴溶液和草酸铵溶液反应制得,写出该反应的离子方程式:
(2)现将含0.5molFeCl3的溶液和含0.5molKSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++SCN-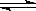 Fe(SCN)2+(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图1所示:则该反应△H 0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45mol /L,求达到平衡时的平均反应速率v(SCN-)= mol·L-1·S-1 ,该温度下的Fe3+的平衡转化率为 ,该温度下反应的平衡常数为 。
Fe(SCN)2+(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图1所示:则该反应△H 0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45mol /L,求达到平衡时的平均反应速率v(SCN-)= mol·L-1·S-1 ,该温度下的Fe3+的平衡转化率为 ,该温度下反应的平衡常数为 。

(3)已知某溶液中,Co2+、Ni2+的浓度分别为0.60mol/L和1.2mol/L,取一定量的该溶液,向其中滴加NaOH溶液,当Co(OH)2开始沉淀时,溶液中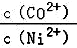 的值等于 .(取两位有效数字)(已知Ksp[Co(OH)2]=6.0×10﹣15,Ksp[Ni(OH)2]=2.0×10﹣15)
的值等于 .(取两位有效数字)(已知Ksp[Co(OH)2]=6.0×10﹣15,Ksp[Ni(OH)2]=2.0×10﹣15)
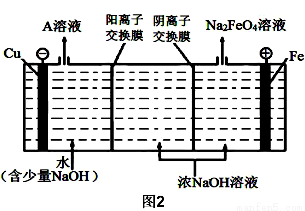
(4)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示,则阳极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期9.18周考化学试卷(解析版) 题型:实验题
硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化
II.SnCl2易水解生成碱式氧化亚锡,Sn相对原子质量为119。
回答下列问题:
(1)锡原子的核电荷数为50,与碳元素属于同一主族,锡元素在周期表中的位置是______。
(2)操作I是________________。
(3) SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因____________。
(4)加入Sn粉的作用有两个:①调节溶液:②______________。
(5)反应I中发生反应的离子方程式为:________。
(6)酸性条件下,SnSO4还可以用作H2O2去除剂,发生反应的离子方程式是:_______。
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为Sn+2HCl=SnCl2+H2↑
②加入过量的FeCl3
③用已知浓度的K2Cr2O7,滴定生成的Fe2+,发生的反应为:Sn+2HCl=6FeCl3+2KCl+2CrCl3+7H2O
取1.226g锡粉,经上述各步反应后,共用去0.100mol/L K2Cr2O7溶液32.0mL。锡粉中锡的质量分数是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com