
��450�沢�д��������£������Ϊ1L���ܱպ��������У���������������������·�Ӧ��2SO2+O2 2SO3
2SO3
��1����֪��64g SO2��ȫת��ΪSO3��ų�85kJ������SO2ת��ΪSO3���Ȼ�ѧ����ʽ�� ��
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK= ��
��3�������¶ȣ���ѧ��Ӧ�ٶ� ���÷�ӦKֵ�� ��ѹǿ�� ���������С�����䡱��
��4��450��ʱ����һ�ܱ������У�������������������ϣ���Ӧ������SO2��O2��SO3���ʵ����仯��ͼ����Ӧ����ƽ��״̬��ʱ����� ��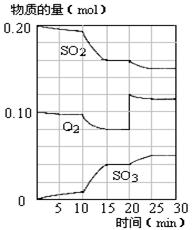
a��10-15min b��15-20min c��20-25min d��25-30min
��5����ͼ�жϣ�10min��15min�����߱仯��ԭ������� ����д��ţ���
a������SO3�����ʵ��� b����С������� c�������¶� d.����
��6����15����ʱ��SO2��ת������ ��
��1��SO2(g)+ O2(g) = SO3(g)����H = -85kJ/mol����2��
O2(g) = SO3(g)����H = -85kJ/mol����2��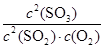
��3������������4��b d��5��c��6��20%
���������������1��������֪��64g SO2Ϊ1mol����ȫת��ΪSO3��ų�����85kJ�������Ȼ�ѧ��Ӧ����ʽSO2(g)+ O2(g)=SO3(g)����H = -85kJ/mol����2�����ݻ�ѧƽ�ⳣ������ʽ����K=
O2(g)=SO3(g)����H = -85kJ/mol����2�����ݻ�ѧƽ�ⳣ������ʽ����K=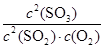 ��3���������Ȼ�ѧ��Ӧ����ʽ������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ�����ѹǿ��С��ƽ�ⳣ��k�������¶ȷ�Ӧ���ʼ�С��4����ƽ��״̬�����������ʵ���Ũ�Ȳ��ٱ仯����ͼ���б���Ϊ���ߣ���bd��ȷ��5����10min��15min�����߱仯��֪��Ӧ�����ʵ����������������ʵ������ߣ���Ӧ������У�����ab�·�Ӧ������У�����c�·�Ӧ������У�����d�²��ı����ʵ����仯����c��ȷ��6��������֪����15����ʱ����Ӧ��SO2���ʵ���Ϊ0.04mol����ʼ���ʵ���Ϊ0.2mol����SO2��ת����Ϊ20%��
��3���������Ȼ�ѧ��Ӧ����ʽ������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ�����ѹǿ��С��ƽ�ⳣ��k�������¶ȷ�Ӧ���ʼ�С��4����ƽ��״̬�����������ʵ���Ũ�Ȳ��ٱ仯����ͼ���б���Ϊ���ߣ���bd��ȷ��5����10min��15min�����߱仯��֪��Ӧ�����ʵ����������������ʵ������ߣ���Ӧ������У�����ab�·�Ӧ������У�����c�·�Ӧ������У�����d�²��ı����ʵ����仯����c��ȷ��6��������֪����15����ʱ����Ӧ��SO2���ʵ���Ϊ0.04mol����ʼ���ʵ���Ϊ0.2mol����SO2��ת����Ϊ20%��
���㣺���ʵ�����Ũ����ʱ��ı仯���ߣ���ѧƽ�⽨���Ĺ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�״���ͨ����ú�������������ɵ�CO��H2��һ�������£��������·�Ӧ�Ƶ�:CO(g)��2H2(g) CH3OH(g)�������ͼʾ�ش��������⣺
CH3OH(g)�������ͼʾ�ش��������⣺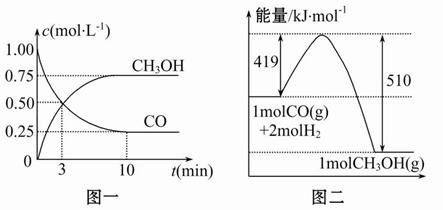
(1)�ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)= ��CO��ת����Ϊ ��
(2)�÷�Ӧ��ƽ�ⳣ������ʽΪ ���¶����ߣ�ƽ�ⳣ�� (���������С�����䡱)��
(3)����һ����ɱ���ܱ������г���1 mol CO��2 mol H2��1 mol CH3OH���ﵽƽ��ʱ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6�������������ʺ�÷�Ӧ�� (����������桱)��Ӧ�����ƶ��������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ�ϲ����ұ���CO2����������Ҫ����ԭ�ϱ���ϩ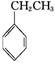 (g)+CO2(g)
(g)+CO2(g)
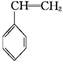 (g)+CO(g)+H2O(g)����H="-166" kJ��mol-1
(g)+CO(g)+H2O(g)����H="-166" kJ��mol-1
(1)���ұ���CO2��Ӧ��ƽ�ⳣ������ʽΪ:K=��������������������������
�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н���,����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬������������(�����)�� 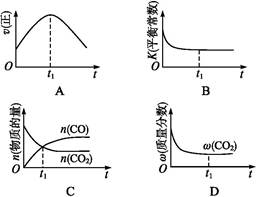
(2)��3 L�ܱ�������,�ұ���CO2�ķ�Ӧ�����ֲ�ͬ�������½���ʵ��,�ұ���CO2����ʼŨ�ȷֱ�Ϊ1.0 mol��L-1��3.0 mol��L-1,����ʵ�����T1��,0.3 MPa,��ʵ���ֱ�ı���ʵ����������;�ұ���Ũ����ʱ��ı仯��ͼ1��ʾ��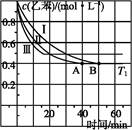
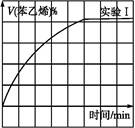
ͼ1 ͼ2
��ʵ����ұ���0~50 minʱ�ķ�Ӧ����Ϊ����������
��ʵ�����ܸı����������������������
��ͼ2��ʵ����б���ϩ�������V%��ʱ��t�ı仯����,����ͼ2�в���ʵ����б���ϩ�������V%��ʱ��t�ı仯���ߡ�
(3)��ʵ����н��ұ�����ʼŨ�ȸ�Ϊ1.2 mol��L-1,������������,�ұ���ת���ʽ���������(�������С�����䡱),�����ʱƽ�ⳣ��Ϊ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) 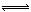 CH3OH(g)��
CH3OH(g)��
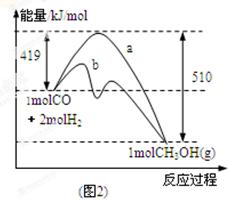
��1��ͼ1�DZ�ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯������ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾƽ����Ӧ����v(CO)�� �� H2��ƽ��ת����Ϊ_________________________��
��2��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯��д����Ӧ���Ȼ�ѧ����ʽ ��
��3�����¶��£���Ӧƽ�ⳣ��K��______________������ֵ�����¶����ߣ�ƽ�ⳣ��K_________(����������䡱��С��)��
��4�����������£����д�ʩ����ʹ��Ӧ��ϵ��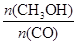 ����Ĵ�ʩ�� ��
����Ĵ�ʩ�� ��
a�������¶� b������He�� c���ٳ���2 molH2 d��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ͼ��ʾ��װ���з�����Ӧ2A2(g)+B2(g)2C(g)����H=" -a" kJ/mol��a ��0������֪P�ǿ����ɻ����Ļ���������ͬ�¶�ʱ�ر�K����A�� B�����зֱ����2mol A2��1mol B2�������ֱ���500��ʱ��ƽ�⣬A��C��Ũ��Ϊw1 mol/L���ų����� b kJ��B��C��Ũ��Ϊw2 mol/L���ų����� c kJ����ش��������⣺
��1���˷�Ӧ��ƽ�ⳣ������ʽΪ______________________�������¶����ߵ�700�棬��Ӧ��ƽ�ⳣ����_____________������С�䣩��
��2���Ƚϴ�С��w1_____ w2���������������a��b��c�ɴ�С�Ĺ�ϵ ______________________��
��3������K��һ��ʱ������´�ƽ�⣬����B�������______________________��������С�䣩��
��4������A��B�������ҹ̶�P����B�иij���4mol A2��2mol B2����500��ʱ��ƽ���C ��Ũ��Ϊw3 mol/L���� w1��w3�Ĺ�ϵ______________________��
��5����˵��A���Ѵﵽƽ��״̬���� ������ţ���һ������ѡ��������⣩��
a��v(C)=2v(B2)
b������������ѹǿ���ֲ���
c�������������ƽ����Է�����������ʱ����仯
d�������ڵ������ܶȱ��ֲ���
��6��ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����_____________��
a����ʱ�����C���� b���ʵ������¶�
c������B2��Ũ�� d��ѡ���Ч�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�̶�������CO2����Ч��������Դ�������ٿ����е��������塣��ҵ����һ����CO�������״�ȼ�ϵķ����� CO2(g)��3H2(g) CH3OH(g)��H2O(g) ��H �� ��49.0 kJ��mol��1��
CH3OH(g)��H2O(g) ��H �� ��49.0 kJ��mol��1��
ij��ѧʵ�齫6molCO2��8molH2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����ͼ��ʾ��ʵ�ߣ���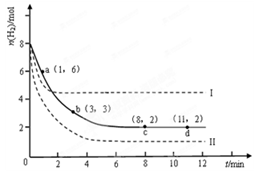
��1��a������Ӧ����_______������ڡ����ڻ�С�ڣ��淴Ӧ���ʡ�
��2������ʱ���ƽ����Ӧ����������__________��
| A��0��1min | B��1��3min | C��3��8min | D��8��11min |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����衣
��֪��SO2��g���� O2��g��
O2��g�� SO3��g�� ��H����98 kJ��mol��1��
SO3��g�� ��H����98 kJ��mol��1��
��1��ij�¶��¸÷�Ӧ��ƽ�ⳣ��K��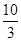 �����ڴ��¶��£���100 L�ĺ����ܱ������У�����3.0 mol SO2(g)��16.0 mol O2(g)��3.0 mol SO3(g)����Ӧ��ʼʱv������ v���棩�����������������������
�����ڴ��¶��£���100 L�ĺ����ܱ������У�����3.0 mol SO2(g)��16.0 mol O2(g)��3.0 mol SO3(g)����Ӧ��ʼʱv������ v���棩�����������������������
��2��һ���¶��£���һ�����������Ϊ2 L���ܱ������г���2.0 mol SO2��1.0 molO2���ﵽƽ��������Ϊ1.6 L����SO2��ƽ��ת����Ϊ ��
��3���ڣ�2���еķ�Ӧ�ﵽƽ��ı�������������ʹSO2(g)ƽ��Ũ�ȱ�ԭ����С���� ������ĸ����
| A�������¶Ⱥ�����������䣬����1.0 mol O2 |
| B�������¶Ⱥ�������ѹǿ���䣬����1.0 mol SO3 |
| C�������¶� |
| D���ƶ�����ѹ������ |
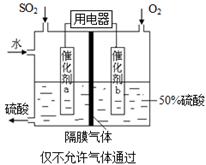
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ж������������N2O5��һ�������������������ʺ��Ʊ��յ����ǵĹ�ע��
��1��һ���¶��£��ں����ܱ�������N2O5�ɷ������з�Ӧ��2N2O5(g) 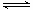 4NO2(g)��O2(g) ���SH��0
4NO2(g)��O2(g) ���SH��0
�ٷ�Ӧ�ﵽƽ�������ͨ��һ�����������N2O5��ת���ʽ�___�����������С���������䡱����
���±�Ϊ��Ӧ��T1�¶��µIJ���ʵ�����ݣ�
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol��L��1 | 5.00 | 3.52 | 2.48 |
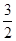 ��(������NO2�ۺϳ�N2O4)����N2O5��ת����a1�� �����¶��·�Ӧ��ƽ�ⳣ��K��_______��
��(������NO2�ۺϳ�N2O4)����N2O5��ת����a1�� �����¶��·�Ӧ��ƽ�ⳣ��K��_______��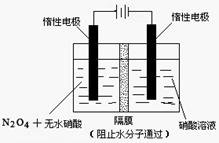
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������������ʡ����ᡢ����ȵ���Ҫԭ�ϡ�
��1��ʵ����ģ��ϳɰ����ں��º����ܱ������а��ռס��ҡ������ַ�ʽ�ֱ�Ͷ�ϣ���λ��mol /L����ƽ��ʱ��ü�������H2��ת����Ϊ20%��
| | N2 | H2 | NH3 |
| �� | 1 | 3 | 0 |
| �� | 0.5 | 1.5 | 1 |
| �� | 0 | 0 | 4 |
 CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�| T / �� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
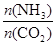 ��x����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
��x����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��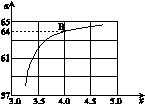
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com