
 氢气是一种理想的“绿色能源”,利用氢能需选择合适的储氢材料.目前正在研究和使用的储氢材料有镁系合金、稀土系合金等.
氢气是一种理想的“绿色能源”,利用氢能需选择合适的储氢材料.目前正在研究和使用的储氢材料有镁系合金、稀土系合金等. (g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$
(g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$ (g)+3H2(g)
(g)+3H2(g)分析 (1)根据LaNi5(s)+3H2(g)?LaNi5H6(s)△H<0,欲使LaNi5H6 (s)释放出气态氢,则平衡向逆向移动,据此分析;
(2)①依据平衡常数表达式解答;
②该实验的目的是储氢,所以阴极上发生的反应为生产目标产物,阴极上苯得电子和氢离子生成环己烷.
解答 解:(1)欲使LaNi5H6 (s)释放出气态氢,则平衡向逆向移动,由LaNi5(s)+3H2(g)?LaNi5H6(s)△H<0为气体减小的放热反应,所以可以升高温度或降低压强,平衡向逆向移动;
故答案为:bc;
(4)①环己烷的起始浓度为amol•L-1,平衡时苯的浓度为bmol•L-1,同一容器中各物质反应的物质的量浓度之比等于其计量数之比,所以根据方程式知,环己烷的平衡浓度为(a-b)mol/L,氢气的浓度为3bmol/L,则平衡常数K=$\frac{C(C{\;}_{6}H{\;}_{6})C{\;}^{3}(H{\;}_{2})}{C(C{\;}_{6}H{\;}_{12})}$=$\frac{27b{\;}^{4}}{a-b}$mol3•L-3;
故答案为:$\frac{27b{\;}^{4}}{a-b}$mol3•L-3;
该实验的目的是储氢,所以阴极上发生的反应为生产目标产物,电解池阴极与电源负极相连,得出电解过程中产生的气体F为O2,阴极上苯得电子和氢离子生成环己烷,电极反应式为C6H6+6H++6e-=C6H12,
故答案为:负;C6H6+6H++6e-=C6H12.
点评 本题考查了化学平衡及其电解池原理等知识点,题目难度较大,注意对相关知识的理解.


科目:高中化学 来源: 题型:选择题
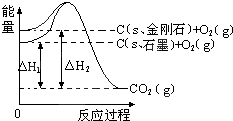
| A. | 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | C(s、石墨)═C(s、金刚石)△H=+1.9 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CO32-)>c(H2CO3) | B. | c(Na+)>c(HCO3-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=2[c(H2CO3)+c(HCO3)+c(CO32-)] | D. | c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请回答:
请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 乙醇氧化制乙醛的实验装置如图所示(夹持仪器和加热仪器均未画出),下列叙述错误的是( )
乙醇氧化制乙醛的实验装置如图所示(夹持仪器和加热仪器均未画出),下列叙述错误的是( )| A. | a中所盛的固体可以是CuO | |
| B. | d中乙醇可用沸水浴加热 | |
| C. | c处具支试管b中有无色液体产生 | |
| D. | c处具支试管b可换成带塞的普通试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| Y | H2SO4 | Fe2O3 | C2H5OH | FeCl3 |
| W | MgSO4 | Al2O3 | C2H5ONa | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com