


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④⑤ | B、①②③ |
| C、②③④ | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙炔能使溴的四氯化碳溶液退色,发生的是取代反应 |
| B、CH2═CH2能使酸性高锰酸钾溶液退色,发生的是氧化反应 |
| C、一氯甲烷在一定条件下即能发生水解反应也能发生消去反应 |
| D、甲苯能使酸性高锰酸钾溶液退色,说明甲苯中含碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.8L0.4mol/L的NaOH溶液 |
| B、0.2L0.15mol/L的Na3PO4溶液 |
| C、1L0.3mol/L的NaCl溶液 |
| D、4L0.5mol/L的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 +HO-NO2 +HO-NO2
 +H2O;取代反应 +H2O;取代反应 | |||
| B、CH2=CH2+Br2→CH2Br-CH2Br;加成反应 | |||
C、2CH3CH2OH+O2
| |||
D、CH3COOH+CH3CH2OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,224mLO2与钠完全反应转化为过氧化钠得到电子数为0.04NA |
| B、在标准状况时,20mLNH3与60mL N2所含的分子个数为1:3 |
| C、将80g NaOH溶于1L水中,所得溶液中 NaOH的物质的量浓度为2moL/L |
| D、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
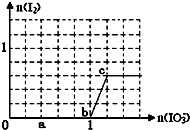 已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A、0~b间反应:3HSO3-+IO3-=3SO42-+I-+3H+ |
| B、a点时消耗NaHSO3的物质的量为1.2 mol |
| C、b~c间反应:I2仅是氧化产物 |
| D、c点之后碘的物质的量不变是因为还原剂消耗完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据能否发生丁达尔效应将分散系分为浊液、溶液和胶体 |
| B、在Fe(OH)3胶体中加入过量盐酸不溶解 |
| C、“血液透析”原理同溶液中固体颗粒的过滤原理相似 |
| D、除加入电解质可使胶体聚沉外,将两种带相反电荷胶粒的胶体混合也能发生聚沉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com