
| A. | 加入催化剂,平衡常数不变 | |
| B. | 减小容器体积,正反应速率增大、逆反应速率减小 | |
| C. | 增大CO(NH2)2的量,CO2的转化率减小 | |
| D. | 降低温度,平衡向逆反应方向移动 |
分析 A.催化剂改变化学反应速率,不改变化学平衡;
B.减小容器体积相当于增大压强,反应速率增大;
C.固体对化学平衡无影响;
D.反应是放热反应,降低温度,平衡正向进行.
解答 解:A.催化剂改变化学反应速率,不改变化学平衡,加入催化剂,平衡常数不变,故A正确;
B.减小容器体积相当于增大压强,反应速率增大,正逆反应速率都增大,故B错误;
C.固体对化学平衡无影响,增大CO(NH2)2的量,CO2的转化率不变,故C错误;
D.依据化学平衡移动原理分析,反应是放热反应,降低温度,平衡正向进行,故D错误;
故选A.
点评 本题考查了化学平衡影响因素分析判断,平衡移动原理的理解应用,注意反应特征的方向,掌握基础是关键,题目较简单.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
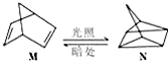 △H=+88.6kJ/mol
△H=+88.6kJ/mol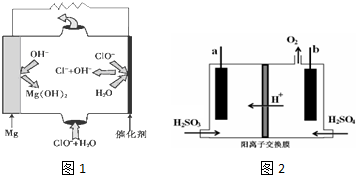
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
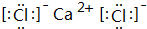 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
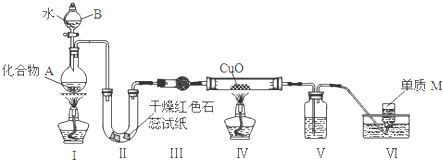
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应生成2mol氯化氢气体,吸收248KJ的能量 | |
| B. | 反应生成2mol氯化氢气体,放出183KJ的能量 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 该反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1.12L CCl4中含有C-Cl键数目为0.2NA | |
| B. | 标准状况下,2.24L氯气中含有${\;}_{17}^{35}$Cl数目一定为0.2NA | |
| C. | 常温常压下,4.4g CO2与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 80 mL 10 mol•L-1 盐酸与足量MnO2加热反应,产生Cl2的体积为4.48L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去甲烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| B. | 苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环结构 | |
| C. | 乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应 | |
| D. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com