
科目:高中化学 来源: 题型:
有关氯水的下列叙述中,正确的是( )
A.新制氯水中只有Cl2和H2O两种分子
B.新制氯水可使蓝色石蕊试纸先变红后退色
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后,酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
空气吹出法是最早工业化海水提溴的方法,适合从低浓度含溴溶液中提取溴。
 |
(1)NaBr的电子式是 。
(2)反应①是将Br—转化为Br2,反应①的离子方程式是 。
(3)通入空气吹出Br2,并用Na2CO3吸收的目的是 。
(4)反应②的化学方程式是 。
(5)反应③中每生成3 mol Br2,转移电子的物质的量是 mol。
(6)为了除去工业Br2中微量的Cl2,可向工业Br2中 (填字母)。
a.通入HBr b.加入NaBr溶液 c.加入Na2CO3溶液 d.加入Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.乙炔分子中,每个碳原子都有两个未杂化的2p轨道形成π键
B.sp3杂化轨道是由能量相近1个s轨道和3个p轨道混合形成的四个sp3杂化轨道
C.凡中心原子采取sp2杂化的分子,其分子构型都是平面三角形
D.氨气分子中有一对未参与杂化的孤对电子
查看答案和解析>>
科目:高中化学 来源: 题型:
图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2)。分子内存在空腔,能嵌入某微粒并形成4个氢键予以识别。下列微粒中,能被该有机化合物识别的是
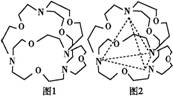
A.CF4 B.CH4 C.NH4+ D.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
硅是重要的半导体材料,构成了现代电子工业的基础。
(1)基态Si原子中,电子占据的最高能层符号为____________。
(2)硅也有系列氢化物-----硅烷,SiH4分子中H原子的1s轨道与Si原子的__________轨道重叠形成Si—H σ键。
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,这种变化关系原因是
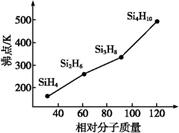
___________________________________________________________________________。
(4)科学家们在高温高压下将CO2制成与SiO2结构类似的新型CO2晶体。这种新型CO2晶体与SiO2相比,熔点更高的是____________________;原因是__________________
___________________________________________________________________________。
(5)在硅酸盐中,Si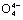 四面体[如下图(a)]通过共用顶角氧离子可形成多种结构型式。图(b)为一种无限长单链结构的多硅酸根X;
四面体[如下图(a)]通过共用顶角氧离子可形成多种结构型式。图(b)为一种无限长单链结构的多硅酸根X;
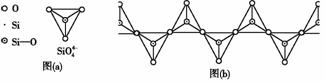
X中Si与O的原子数之比为________________,化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列烷烃:①正己烷 ②丙烷 ③正戊烷 ④正丁烷 ⑤癸烷中,沸点由高到低的顺序正确的是( )
A.①②③④⑤ B.⑤①③④② C.⑤③④①② D.③④⑤②①
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,体积均为0. 25L的两个恒容密闭容器中发生可逆反应:N2 (g)+3H2 (g)  2NH3 (g)
2NH3 (g)
△H= - 92. 6kJ/moL。实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系 能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器②中达平衡时放出的热量Q=23. 15kJ
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器①、②中反应的平衡常数相等
D.若容器①体积为0. 5L,则平衡时放出的热量小于23. 15kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com