
【题目】
A. 先用稀NaOH溶液洗,再用水冲洗 B. 先用水洗,再用酒精冲洗
C. 先用酒精洗,再用水冲洗 D. 用布擦去后再用水冲洗
科目:高中化学 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:
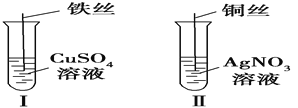
①Ⅰ中发生反应的离子方程式为___________________________________;
②Ⅱ中铜丝上观察到的现象是______________________________________
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为__________。
(2)将少量Cl2通入FeCl2的溶液中,反应的离子方程式为2Fe2++Cl2===2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱为___________________
(3) NaHCO3溶液与足量澄清石灰水反应的离子方程式_____________________________
(4)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。
①写出反应方程式并标出电子转移方向及数目______________________________________
②若反应方程式中转移了0.3 mol电子,则氧化产物的质量是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为___________(用名称表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式:___________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是______________。
① 硫酸铝和氢氧化钠 ② 硫酸锌和氢氧化钠 ③硫酸铝和氨水 ④ 硫酸锌和氨水
(4)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另一种耐高温的物质,写出该反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:

(1)若A、B、C的焰色反应均为黄色,C为厨房中的用品,D的过度排放会造成温室效应。
①A的化学式______________、B的俗名____________;
②反应II的离子方程式是__________________________________。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①反应II的离子方程式是_____________________________;
②反应Ⅲ的离子方程式是_____________________________;
③检验B中阳离子最好的方法是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表没食子儿茶素没食子酸酯(EGCG)是中国绿茶中主要的活性成份,下列说法正确的是

A. 分子式为C22H20O11
B. 分子只有1个手性碳原子
C. 分子易发生氧化反应,因此绿茶具有抗氧化性
D. 1mol该化合物与足量的NaOH溶液反应,最多消耗10molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.5 mol Cu2S和足量稀HNO3反应,生成Cu(NO3)2、H2SO4、NO和H2O。则参加反应的硝酸中被还原的硝酸的物质的量是
A. 5 mol B. 1.5 mol C. 6 mol D. 1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物脱H2S的原理为:
反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,氧化速率随温度和pH变化如下图。下列说法正确的是

A. 该过程最终将H2S转化为Fe2(SO4)3
B. H+是反应2的反应物,c(H+)越大反应速率越快
C. 反应1消耗11.2LH2S,转移的电子数目约为6.0×1023个
D. 反应温度过高,Fe2+氧化速率下降,其原因可能是硫感菌失去活性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中与盐类的水解有关的是 ( )
A. 自来水杀菌、消毒B. 盛放Na2CO3溶液的试剂瓶应用橡皮塞
C. 铁在潮湿的环境下生锈D. 酸雨在空气中放置一段时间后,pH降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com