
【题目】科学家们已研发出硅负极锂离子电池,在相同体积中,硅负极电池容量比石墨碳电池容量提升25%,反应原理为5LiMn2O4+Si![]() 5Li0.12Mn2O4+Li4.4Si,LiPF6纯液体作电解质,下列有关说法正确的是( )
5Li0.12Mn2O4+Li4.4Si,LiPF6纯液体作电解质,下列有关说法正确的是( )
A.放电时的负极反应为Li﹣e﹣=Li+
B.若用该电池电解水,阴极生成3.52gO2,则该电池负极质量减少0.77g
C.锂离子电池充电时的阴极反应为Si+4.4e-+4.4Li+=Li4.4Si
D.放电时电解质LiPF6水溶液中的Li+移向正极
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】二草酸合铜( II )酸钾晶体{K2[Cu(C2O4)2]·2H2O},微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。
I.用氧化铜和草酸为原料制备二草酸合铜(II)酸钾晶体的流程如下:
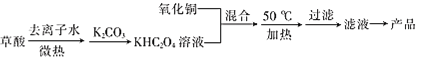
已知:H2C2O4![]() CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
回答下列问题:
(1)将H2C2O4晶体加入去离子水中,微热,溶解过程中温度不能太高,原因是________。
(2)将CuO与KHC2O4的混合液在50°C下充分反应,该反应的化学方程式为__________。
(3)50 °C时,加热至反应充分后的操作是_______________(填字母)。
A.放于冰水中冷却后过滤 B.自然冷却后过滤
C.趁热过滤 D.蒸发浓缩、冷却后过滤
II.以CuSO4·5H2O晶体和K2C2O4固体为原料制备二草酸合铜( II )酸钾晶体。
实验步骤:将CuSO4·5H2O晶体和K2C2O4固体分别用去离子水溶解后,将K2C2O4溶液逐滴加入硫酸铜溶液中,有晶体析出后放在冰水中冷却,过滤,用酒精洗涤,在水浴锅上炒干。炒时不断搅拌,得到产品。
(4)用酒精而不用冷水洗涤的目的是____________。
II.产品纯度的测定:准确称取制得的晶体试样ag溶于NH3·H2O中,并加水定容至250mL,取试样溶液25.00mL,再加入10 mL的稀硫酸,用b mol·L-1 的KMnO4标准液滴定,消耗KMnO4标准液V mL。
(5)滴定时,下列滴定方式中,最合理的是______(填字母),理由为________。 (夹持部分略去)
A. 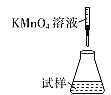 B.
B. 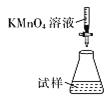 C.
C. 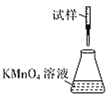
(6)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,实验结果会_____(填“偏大”偏小”或“无影响”)。
(7)该产品的纯度为___________(写出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g) ![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积增大
A. ①②B. ①③C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,3,5-三溴苯甲酸(H)是一种新型植物生长调节剂,应用于农作物,具有高效、低毒、调节作物生长、增产效果明显等特性。其合成路线如图所示:
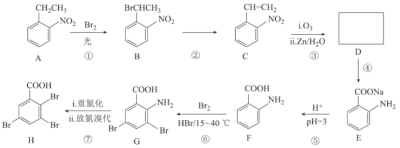
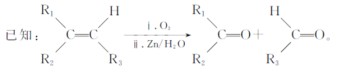
回答下列问题:
(1)反应①的反应类型为__。
(2)写出反应②所需的试剂和条件:__。
(3)同时满足下列条件的B的同分异构体有__种(不含立体异构),任写其中一种结构简式:__。
i.属于芳香族化合物,且官能团种类与B相同。
ii.核磁共振氢谱显示有4组峰,且峰面积之比为1:1:1:1。
(4)D的结构简式为__。
(5)H中所含官能团的名称为__。
(6)写出反应⑥的化学方程式:__。
(7)参照上述合成路线和信息,设计由1-丁烯(无机试剂任选)制备丙酸甲酯的合成路线:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是( )
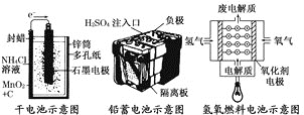
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,石墨电极变细
C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)[化学——选修5:有机化学基础]
近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物Y,其合成路线如下:
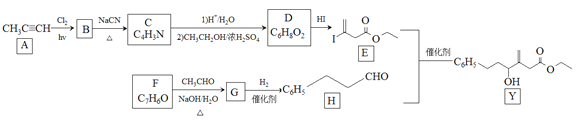
已知:![]()
回答下列问题:
(1)A的化学名称是________________。
(2)B为单氯代烃,由B生成C的化学方程式为________________。
(3)由A生成B、G生成H的反应类型分别是________________、________________。
(4)D的结构简式为________________。
(5)Y中含氧官能团的名称为________________。
(6)E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为________________。
(7)X与D互为同分异构体,且具有完全相同官能团。X的核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为3∶3∶2。写出3种符合上述条件的X的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
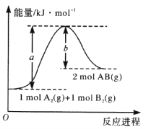
A. 每生成2 mol AB吸收bkJ热量
B. 该反应热△H= + (a-b)kJ mol-1
C. 该反应中反应物的总能量高于生成物的总能量
D. 断裂1 mol A—A和1 mol B—B键,放出akJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g)![]() 2C(g)+zD(g)若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g)若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=v(D)=0.25 mol·L-1·s-1
B.z=3
C.B的转化率为25%
D.C的体积分数为20%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com