
| A、标准状况下,46g NO2中含有的分子数为NA |
| B、通常状况下,14g CO含有的电子数目为7NA |
| C、1L 0.2 mol/L的CH3COOH溶液中,H+数目为0.2NA |
| D、0.1mol Cu 和与40mL 10mol/L硝酸反应后,溶液中的NO3-数目为0.2NA |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
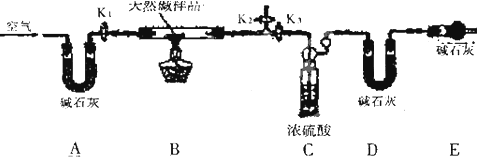
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe-3e-=Fe3+ |
| B、O2+2H2O+4e-=4OH- |
| C、Fe-2e-=Fe2+ |
| D、O2+2H2O-4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、燃料电池工作时,正极反应为:O2+2H2O+4e-═4OH- |
| B、在溶液中SO42-往b极移动 |
| C、若a、b极都是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D、若a极是铜,b极是铁时,a极逐渐溶解,b极上有铜析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 异常情况 | 可能的原因 |
| ① | 蒸发结晶时,蒸发皿破裂 | 将溶液蒸干或酒精灯灯芯碰到蒸发皿底部 |
| ② | 粗盐水过滤后,滤液仍浑浊 | 滤纸与漏斗内壁间有气泡 |
| ③ | 萃取时,振荡溶液,静置不分层 | 萃取剂加得太多 |
| ④ | 蒸馏时,发现冷凝管破裂 | 没有通冷凝水或先加热后通冷凝水 |
| A、①②③④ | B、②③④ |
| C、②③ | D、② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KMnO4 |
| B、过量Cl2 |
| C、FeCl3 |
| D、FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、碳棒上有气体放出,溶液pH值变大 |
| B、a是正极,b是负极 |
| C、导线中有电子流动,电子从a极到b极 |
| D、a极上发生了氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com