
【题目】呋喃甲酸俗称糠酸,广泛应用于塑料工业、食品行业、涂料、医药、香料等。用呋喃甲醛制备呋喃甲酸和副产品呋喃甲醇的原理为:
反应1:![]() +NaOH
+NaOH![]()
![]() △H<0
△H<0
反应2:![]() +HCl
+HCl![]()
![]() +HCl
+HCl
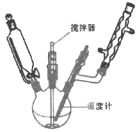
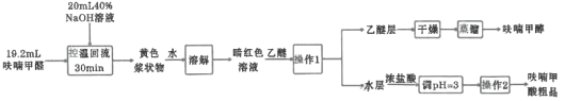
某研究性学习小组利用上图装置制备呋喃甲酸的实验流程如下:
已知:①乙醚(![]() )沸点34.6℃,其蒸气有毒,可使人失去知觉。
)沸点34.6℃,其蒸气有毒,可使人失去知觉。
②主要试剂相关物理性质如下:
试剂 | 相对分子质量 | 密度/ | 熔点/℃ | 沸点/℃ | 溶解性 |
呋喃甲醛 | 96 | 1.16 |
| 161.7 | 微溶于水,易溶于乙醇、乙醚。 |
呋喃甲醇 | 98 | 1.13 |
| 171.0 | 溶于水,可混溶于乙醇、乙醚。 |
呋喃甲酸 | 112 | - | 129.5 | 231.0 | 微溶于冷水,在热水中溶解度较大,易溶于乙醇、乙醚。 |
请回答下列问题:
(1)“控温回流”时需控制反应温度8~12℃,应采取的控温方式是________,三颈烧瓶中所加入的![]() 溶液应如何预处理________,滴加呋喃甲醛时需________。
溶液应如何预处理________,滴加呋喃甲醛时需________。
(2)在“控温回流”时充分搅拌才能获得较高产率。其原因是________。
(3)“操作1”的名称为________,所用到的玻璃仪器主要有________,“操作2”主要包括________、________。
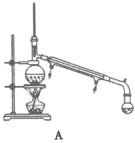
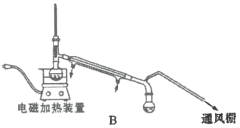
(4)“蒸馏”时,用下图________(填字母标号)装置更好,与另一装置相比,该装置的优点有①________;②________。
(5)呋喃甲酸粗品精制所采用的方法是________,最终得到精产品9.86g,呋喃甲酸的产率为________。
【答案】冷水浴 在略低于8℃的冷水浴中冷却 缓慢(滴加) 反应在两相中进行,不断搅拌使反应物充分接触 萃取分液 分液漏斗与烧杯 过滤 洗涤 B 及时排出乙醚蒸气,以免中毒 无明火加热,可防止乙醚蒸气燃爆 重结晶 75.9%
【解析】
由流程图可知,呋喃甲醛与NaOH反应发生歧化,生成呋喃甲醇和呋喃甲酸钠,加水后二者都溶解,加乙醚萃取,呋喃甲醇进入乙醚层,呋喃甲酸钠进入水层。乙醚层经干燥蒸馏得到呋喃甲醇,水层加浓盐酸,呋喃甲酸转化为呋喃甲酸,经过滤洗涤得到呋喃甲酸粗品。
(1)化学上常用的控温方式是水浴和油浴,控制反应温度8~12℃需要用冷水浴;由于反应在8~12℃条件下进行,加入的NaOH溶液需提前冷却一下,防止使体系温度过高,故加之前要在略低于8℃的冷水浴中冷却;由于呋喃甲醛与NaOH的反应放热,为了控制温度在8~12℃,滴加呋喃甲醛时需缓慢滴加;
(2)呋喃甲醛微溶于水,而NaOH在水层中,两相互不相溶,为了使二者充分接触发生反应,需要不断搅拌;
(3)操作1是使水层和有机层分开,是萃取分液操作;用到的玻璃仪器有分液漏斗与烧杯;根据分析,操作2是分离固体和液体,是过滤、洗涤;
(4)乙醚等有机物易挥发且易燃,装置B使用电加热,没有明火,避免发生危险,且在通风橱中进行,及时排出乙醚蒸气,以免中毒,故使用B装置;
(5)固体物质提纯,可将其溶解后重新结晶,即用重结晶法;加入呋喃甲醛的质量为19.2mL×1.16g/mL=22.272g,物质的量为![]() ,故理论生成呋喃甲酸的物质的量为
,故理论生成呋喃甲酸的物质的量为![]() 0.232mol=0.116mol,质量为0.116mol×112g/mol=12.992g,产率为
0.232mol=0.116mol,质量为0.116mol×112g/mol=12.992g,产率为![]() ;
;


科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 为短周期元素,其原子半径、化合价等信息见下表。以下说法一定正确的是( )
为短周期元素,其原子半径、化合价等信息见下表。以下说法一定正确的是( )
元素 |
|
|
|
|
原子半径( | 0.077 | 0.070 | 0.104 | 0.099 |
最高正价或最低负价 | +4 | +5 | -2 | -1 |
A.![]() 与
与![]() 形成的化合物的电子式可表示为
形成的化合物的电子式可表示为![]()
B.![]() 的氢化物能与
的氢化物能与![]() 的氢化物反应,所得产物只含有共价键
的氢化物反应,所得产物只含有共价键
C.![]() 、
、![]() 能分别与氧元素形成多种氧化物
能分别与氧元素形成多种氧化物
D.![]() 处于元素同期中第三周期ⅣA族
处于元素同期中第三周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将充满NO2和O2的试管倒立于水槽中,充分反应后,剩余气体的体积为原混合气体体积的![]() ,则原混合气体中NO2和O2的体积之比是
,则原混合气体中NO2和O2的体积之比是
A.8:1B.7:3C.1:7D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
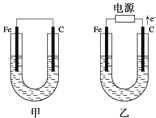
(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的___棒,乙池中的___棒。
②乙池中阳极的电极反应式是___。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式___。
②甲池中碳极上电极反应式是___,乙池碳极上电极反应属于___(填“氧化反应”或“还原反应”)。
③将湿润的KI淀粉试纸放在乙池碳极附近,发现试纸变蓝,反应的化学方程式为___。
④若乙池转移0.02mole﹣后停止实验,池中电解质溶液体积是200mL,则溶液混合均匀后的pH=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如图所示,回答下列问题。

(1)加入过量A溶解后,在进行操作a时玻璃棒的作用是______________________。
(2)工厂废液中加入过量A的目的是______________________________。
(3)溶液甲中的金属离子是_____________________(写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是________(填序号)。
(5)步骤③中发生反应的化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在元素周期表中的相对位置如下图所示,其中Z元素原子之间通常形成Z2分子。下列说法不正确的是( )
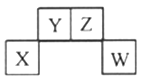
A. X元素的单质既能与强酸反应也能与强碱反应
B. Y元素形成的氢化物在常温下不一定为气体
C. W元素的最高价氧化物对应水化物一定为强酸
D. 由Y、Z、W三种元素形成的二元化合物中只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为易挥发液体,C为气体。
D、E、F、G、X均为化合物,其中X是一种无氧强酸、E为黑色固体,H在常温下为液体.它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
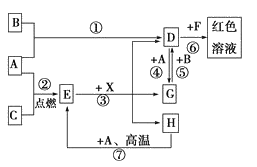
(1)写出化学式:A___,D___,E___,X___。
(2)在反应①~⑦中,不属于氧化还原反应的是____。(填编号)
(3)反应⑥的离子方程式为____。
(4)反应⑦的化学方程式为____。
(5)该反应中每消耗0.3mol的A,可转移电子___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)鉴别KCl溶液和K2CO3的试剂是___________,离子方程式为________________。
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是________,离子方程式为___________。
(3)除去Na2CO3粉末中混入的NaHCO3杂质用________方法,化学方程式为_____________。
(4)除去铁粉中混有铝粉的试剂是___________,离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属镁,其流程如下图所示:
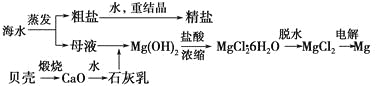
(1)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。__________________________
(2)实验室将粗盐制成精盐的过程中,溶解、过滤、蒸发三个步骤的操作都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
①溶解:________________。
②过滤:__________________________。
③蒸发:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com