
将4.6 g金属钠投入到95.6 g水中,得到的溶液溶质的质量分数为( )。
A.4.6% B.7.6% C.8% D.10%
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
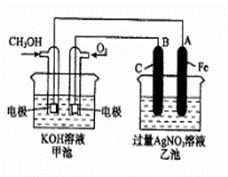
右图是一个化学过程的示意图。已知甲池的总反应式为:
 2CH3OH+3O2+4KOH===2K2CO3+6H2O
2CH3OH+3O2+4KOH===2K2CO3+6H2O
(1)请回答下列电极的名称:通入CH3OH的电极名称是_______________,B(石墨)电极的名称是___________。
(2)写出电极反应式: 通入O2的电极的电极反应式是 __________________________________。A(Fe)电极的电极反应式_______________________________。
(3)乙池中反应的化学方程为 ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组反应,均可用同一离子方程式表示的是 ( )
A.HCl和Na2CO3溶液反应, HCl溶液和CaCO3反应
B.足量稀H2SO4和Na2CO3溶液反应, 足量稀HNO3和K2CO3溶液反应
C.稀H2SO4和Ba(OH)2溶液反应, 稀H2SO4和KOH溶液反应
D.BaCO3和稀 H2SO4溶液反应, BaCO3和稀HCl 溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于焰色反应的表述确切的是( )。
A.焰色反应是元素的性质
B.焰色反应是单质的特有性质
C.焰色反应是离子的特有性质
D.焰色反应是化合物的特有性质
查看答案和解析>>
科目:高中化学 来源: 题型:
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W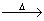 X+H2O+CO2↑ ②Z+CO2—→X+O2
X+H2O+CO2↑ ②Z+CO2—→X+O2
③Z+H2O一→Y+O2↑ ④X+Ca(OH)2—→Y+CaCO3↓
(1)W、X、Y、Z的化学式分别是:W:________、X________、Y________、Z________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式),还原剂是________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:①离子方程式:________。②化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下述对焰色反应实验操作注意事项的说明,正确的是( )。
①钾的火焰颜色要透过蓝色钴玻璃观察 ②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质 ③每次实验后,要将铂丝用盐酸洗净 ④实验时最好选择本身颜色较浅的火焰 ⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确 C.仅有⑤不正确 D.全对
查看答案和解析>>
科目:高中化学 来源: 题型:
“套管实验”是将一支较小的玻璃仪器放入另一玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验。因其具有许多优点,近年被广泛开发并应用于化学实验中。请观察下列实验装置,分析实验原理,并回答下列问题:
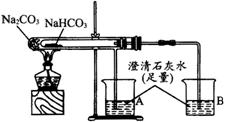
(1)从点燃酒精灯开始,试管及烧杯A、B中能观察到的现象有________________。
(2)整个实验结束时,在操作上需要特别注意的问题是________________。
(3)通过该实验可以得出的结论是(结合化学方程式来说明)________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如下表所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是
| 不纯物质 | 除杂试剂 | 分离方法 | |
| A | 苯(甲苯) | KMnO4(酸化),NaOH溶液 | 分液 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | 乙酸乙酯(乙酸) | KOH溶液,水 | 分液 |
| D | CO3(SO2) | Na2CO3 | 洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(一) A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):
请填写下列空白:
(1)G是 。(用化学式填写)
(2)E与F反应的化学反应方程式是 。
(3)F与G的水溶液的反应生成I和D的离子方程式是 。
 (4)将2.5 g H、I和碳酸氢钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸
(4)将2.5 g H、I和碳酸氢钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸 的体积与产生CO2的体积(标准状况)关系如下图所示:
的体积与产生CO2的体积(标准状况)关系如下图所示:
则物质I的物质的量为_______________mol。
(二)工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯
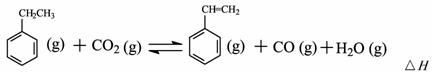 = -166KJ/mol
= -166KJ/mol
(1)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为1.0mol/L和3.0mol/L,其中实验Ⅰ在T1℃,0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图Ⅰ所示。
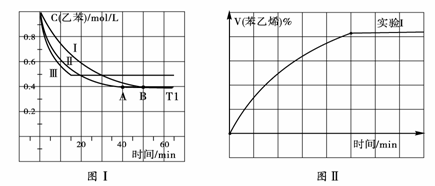
① 实验I乙苯在0—50min时的反应速率为
② 实验Ⅱ可能改变条件的是
③图II是实验Ⅰ中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体
积分数V%随时间t的变化曲线。
(2)若实验Ⅰ中将乙苯的起始浓度改为1.2 mol/L,其他条件不变,乙苯的转化率将 (填“增大”、“减小”或“不变”),计算此时平衡常数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com