
【题目】恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g), 已知反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol; 反应达平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%。则:
2NH3(g), 已知反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol; 反应达平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%。则:
(1)a的值为______。
(2)平衡时NH3的物质的量为___________。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=___________________。
(4)原混合气体中,a∶b=________。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=________。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
【答案】 16 8mol 5∶4 2∶3 1∶2 3∶3∶2
【解析】(1)、根据方程式计算:
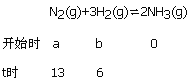
因t时生成6molNH3,则消耗了3molN2,所以a=13+3=16,故答案是:16。
(2)反应达平衡时,混合气体的物质的量为716.8L÷22.4L/mol=32mol,则NH3的物质的量为32mol×25%=8mol;故答案是:8mol。
(3)利用差量法计算:
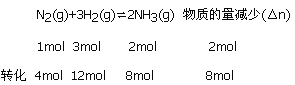
故原混合气体为32mol+8mol=40mol,则原混合气体与平衡混合气体的物质的量之比n(始):n(平)=40mol:32mol=5:4;故答案是5:4。
(4)由(1)知a=16mol,则b=40mol-16mol=24mol,所以a:b=16mol:24mol=2:3;故答案是2:3。
(5)达到平衡时,N2的转化率是α(N2)= ![]() ×100%=25%,H2的转化率α(H2)=
×100%=25%,H2的转化率α(H2)= ![]() ×100%=50%,所以达到平衡时,N2和H2的转化率之比:α(N2)∶α(H2)=25%:50%=1:2;故答案是1:2。
×100%=50%,所以达到平衡时,N2和H2的转化率之比:α(N2)∶α(H2)=25%:50%=1:2;故答案是1:2。
(6)平衡混合气的组成为:n(N2)=16mol-4mol=12mol,n(NH3)=8mol,n(H2)=32mol-12mol-8mol=12mol,平衡混合气体中,n(N2):n(H2):n(NH3)=12mol:12mol:8mol=3:3:2,故答案是3:3:2。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】在N2+3H22NH3的可逆反应中,自反应开始至2s末,氨的浓度由0变为0.8 molL﹣1 则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
A.0.3 molL﹣1S﹣1
B.0.4 molL﹣1S﹣1
C.0.6molL﹣1S﹣1
D.0.8 molL﹣1S﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解质溶液为KOH溶液。下列有关该电池的叙述不正确的是
A. 正极反应式为:O2+2H2O+4e-=4OH-
B. 工作一段时间后,电解质溶液中KOH的物质的量不变
C. 该燃料电池的总反应方程式为:2H2+O2=2H2O
D. 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施符合“绿色化学”思想的是
A. 直接排放含磷生活污水
B. 大量使用氟里昂作为冰箱制冷剂
C. 使用可降解塑料代替不可降解塑料
D. 使用化学性质稳定、不易分解的有机氯农药
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )

A. 有O2放电的a极为电池的负极
B. 有H2放电的b极为电池的负极
C. a极对应的电极反应为O2+2H2O+4e-===4OH-
D. b极对应的电极反应为2H2-4e-+4OH-===4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

请回答:
(1)B极是电源的___________ ,一段时间后,甲中溶液颜色 __________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___________ ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 ______________。
(3)现用丙装置给铜件镀银,则H应该是______________ (填“镀层金属”或“镀件”),电镀液是___________ 溶液(填写化学式)。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为_____________ ,甲中溶液的pH_____________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烯烃为原料,合成某些高聚物的路线如下:
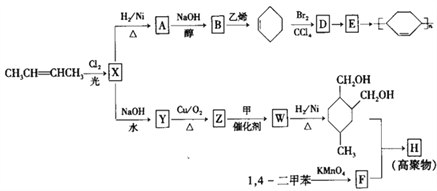
已知: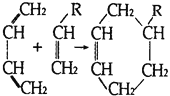 (或写成
(或写成![]() )
)
(1)CH3CH=CHCH3的名称是____________。
(2)X中含有的官能团是______________。
(3)A→B的化学方程式是_____________。
(4)D→E的反应类型是_______________。
(5)甲为烃,F能与NaHCO3反应产生CO2。
①下列有关说法正确的是_______________。
a.有机物Z能发生银镜反应 b.有机物Y与HOCH2CH2OH互为同系物
c.有机物Y的沸点比B低 d.有机物F能与己二胺缩聚成聚合物
②Y的同分异构体有多种,写出分子结构中含有酯基的所有同分异构体的种类数_____。
③Z→W的化学方程式是__________________。
(6)高聚物H的结构简式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaSO4在医疗上可做消化系统造影剂,2mol BaSO4含有的硫原子个数为
A. 2 B. 2×6.02×1023 C. 6 D. 6×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是
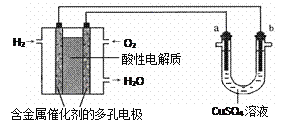
A. 燃料电池工作时,通入氢气的是正极
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com