
【题目】根据海水综合利用的工业流程图,判断下列说法不正确的是( )

A. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
B. 在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 从能量转换角度看,氯碱工业电解饱和食盐水是一个将电能转化为化学能的过程
D. 从第④步到第⑤步的目的是富集Br2
【答案】B
【解析】A、除去粗盐中Mg2+,常用NaOH,除去SO42-,常用BaCl2,除去Ca2+,常用Na2CO3,Na2CO3的作用不仅是除去Ca2+,还要除去过量的BaCl2,因此Na2CO3放在BaCl2的后面,即顺序是NaOH、BaCl2、Na2CO3或者BaCl2、NaOH、Na2CO3或者BaCl2、Na2CO3、NaOH,然后过滤,再加盐酸,除去过量的NaOH和Na2CO3,故A说法正确;B、灼烧MgCl2·6H2O时,需要在HCl氛围中加热,防止Mg2+水解,故B说法正确;C、电解饱和食盐水,此装置为电解池,是电能转化为化学能,故C说法正确;D、海水中Br-浓度低,从④步到⑤步,目的是富集Br2,故D说法正确。


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大最的热。氢气燃烧生成水蒸气的能最变化如下图所示:

根据上图可知,在化学反应中,不仅存在物质的变化,而且伴随着______变化,1molH2完全燃烧生成1molH2O(气态)时,释放的能量是_______kJ。
(2)下列化学反应在理论上可以设计成原电池的是________。
A.Fe+2FeCl3=3FeCl2 B.SO3+H2O=H2SO4
C.CH4+2O2![]() CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
(3)下图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下:

a.电流计指针偏转 |
b.Cu极有H2产生 |
c.H+向负极移动 |
d.电流由Zn经导线流向Cu |
①实验报告中记录合理的是_______(填序号)。
②请写出该电池的负极反应式_________。
③若有1mol电子流过导线,则理论上产生H2的质量为______g.
④将稀H2SO4换成CuSO4溶液,电极质量增加的是______(填“锌极”或“铜极”,下同),溶液中SO42-移向_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应2SO3(g)![]() 2SO2(g)+O2(g),将1molSO3气体通入1L容积恒定的密闭容器中,维持容器内温度不变,5min末测得SO3的物质的量为0.4mol。则下列说法正确的是( )
2SO2(g)+O2(g),将1molSO3气体通入1L容积恒定的密闭容器中,维持容器内温度不变,5min末测得SO3的物质的量为0.4mol。则下列说法正确的是( )
A. 0~5min,O2的生成速率v(O2)=0.06mol·L-1·min-1
B. 若起始时充入3molSO3,起始时SO3分解速率不变
C. 若某时刻消耗了0.5molSO3同时生成了0.25molO2,则表明该反应达到了平衡状态
D. 达到平衡时,SO2和SO3的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CrO42-+2H+![]() Cr2O72-+H2O。25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如下曲线。下列说法不正确的是( )
Cr2O72-+H2O。25℃时,调节初始浓度为1.0mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如下曲线。下列说法不正确的是( )

A. 平衡时,pH越小,c(Cr2O72-)越大
B. A、B两点c(CrO42-)之比为5:2
C. B点CrO42-的平衡转化率为40%
D. 平衡时,若溶液中c(CrO42-)=2c(Cr2O72-),则c(H+)=1.0×10-7mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 11gC3H8与CO2的混合气体中所含碳原子数可能为0.5NA
B. 标准状况下,4.48L甲烷和乙烯的混合气体完全燃烧,产物中所含O-H键数目为0.4NA
C. 4.6gNa与100mL1mol·L-1的盐酸溶液反应,转移电子数目为0.1NA
D. 常温下,1LpH=2的硫酸溶液中由水电离出的H+的数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家成功开发出便携式固体氧化物燃料电池,它以丙烷气体为燃料,空气为氧化剂,电解质是固态氧化物,在熔融状态下能传导O2﹣; 该电池的总反应是C3H8+5O2═3CO2+4H2O,负极反应为C3H8﹣20e﹣+10O2﹣═3CO2+4H2O.下列关于该燃料电池的说法中正确的是( )
A.在熔融电解质中,O2﹣由负极移向正极
B.电池的正极通入丙烷
C.电路中每通过5 mol 电子,约有5.6 L标准状况下的丙烷被完全氧化
D.在电池正极的电极反应为O2﹣4e﹣═2O2﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下下列溶液中确关微粒的物质的量浓度关系正确的是
A. 等物质的量浓度的CuSO4和(NH4)2SO4的混合溶液![]()
B. 0.2 mol/L NaHCO3溶液和0.1 mol/LNaOH溶液等体积相混合:![]()
C. pH=2的盐酸与pH=12的氨水等体积混合![]()
D. 0.1 mol/LCH3COONa溶液中通入HC1气体,至pH=7(溶液体积变化忽略不计):![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:
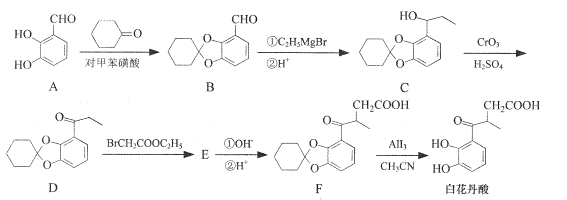
(1)A中的含氧官能团名称为__和_____。
(2)C-D的反应类型为 ___。
(3)白花丹酸分子中混有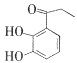 ,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
①分子中有四种不同化学环境的氢;②与FeCl3溶液能发生显色反应,且1 mol该物质最多能与3 mol NaOH反应.
(4)E的结构简式为 ___。
(5)已知:![]() 根据已有知识并结合相关信息写出以
根据已有知识并结合相关信息写出以![]() 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备![]() 的合成路线流程图(合成路线流程图示例见本题题干)____。
的合成路线流程图(合成路线流程图示例见本题题干)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种食品的配料标签如图所示: 
①其中,富含蛋白质的物质是 , 富含油脂的物质是 , 有防腐作用的是 .
②用于包装该食品的聚乙烯塑料包装属于(填字母).
A.有机高分子材料 B.无机非金属材料 C.金属材料
③大量使用塑料包装,会造成“污染”,这种包装袋属于(可回收资源/不可回收资源).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com