
布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
请回答下列问题:
(1)化合物A的分子式为 。
(2)A长期暴露在空气中会变质,其原因是 。
(3)由A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是 (填字母,2分)。
a. b.
b. c.
c. d.
d.
(4)B被H2还原的产物C的结构简式为 。
(5)D→E的化学方程式为: 。
(6)F的结构简式 。
(7)D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是 。
(16分)
(1)C9H9NO(2分) (2)酚类化合物易被空气中的O2氧化(2分)
(3)a (2分)
(4)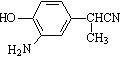 (2分)
(2分)
(5)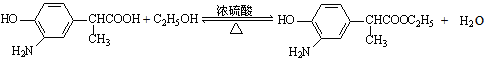 (3分)
(3分)
(6)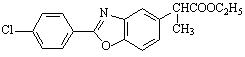 (2分)
(2分)
(7)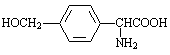 (3分)
(3分)
解析试题分析:(1)合成路线的原料A的结构简式中含有的三种原子团为HO—、—C6H4—、—CH(CH3)CN,则A由9个C、9个H、1个N、1个O原子构成,分子式先写碳、氢,再按英文字母的先后顺序写其它原子,即其分子式为C9H9NO;(2)化合物含有酚羟基,具有酚类物质的性质,部分苯酚被空气中的氧气氧化导致放置时间较长的苯酚由无色变为粉红色晶体,因此部分A也容易被空气中的氧气氧化而变质;(3)由于羟基对苯环上C—H键的活化作用具有定位效应,如苯酚分子中苯环上邻、对位碳所连的氢原子很容易被硝基或溴原子取代,生成邻硝基或邻溴苯酚,而间位碳原子上所连的氢原子则很难被取代,由于A分子中羟基对位碳上已有取代基而无氢原子,则只有邻位碳上所连的氢原子能被硝基继续取代,所以生成的二硝基取代物的结构简式最可能是a选项所代表的有机物;(4)B由HO、NO2、C6H3、CH(CH3)CN构成,则B的分子式为C9H8N2O3,C的分子式为C9H10N2O,对比发现前者比后者多2个O少2个H,由此推断1molB与3molH2发生还原反应,生成1molC和2molH2O,只有硝基变为氨基,其余结构保持不变,由此可以书写该反应的化学方程式,即 ;(5)E由HO、H2N、C6H3、CH(CH3)COOC2H5构成,则E的分子式为C11H15NO3,它比D多2个C、5个H,根据D→E的反应信息及E的结构简式逆推,可以得出D与乙醇在浓硫酸催化下变成E和水的反应是酯化反应,则D的羧基脱去的羟基与乙醇羟基脱去的氢原子结合生成水,其余部分结合生成E,即
;(5)E由HO、H2N、C6H3、CH(CH3)COOC2H5构成,则E的分子式为C11H15NO3,它比D多2个C、5个H,根据D→E的反应信息及E的结构简式逆推,可以得出D与乙醇在浓硫酸催化下变成E和水的反应是酯化反应,则D的羧基脱去的羟基与乙醇羟基脱去的氢原子结合生成水,其余部分结合生成E,即 ;(6)由G的结构简式可知其分子式为C16H12NO3Cl,F的分子式为C18H16NO3Cl,F比G多2个C、4个H,结合反应条件推断,F中酯基发生水解反应,所得有机产物酸化得到的含有羧基的G,由此推断F的结构简式为
;(6)由G的结构简式可知其分子式为C16H12NO3Cl,F的分子式为C18H16NO3Cl,F比G多2个C、4个H,结合反应条件推断,F中酯基发生水解反应,所得有机产物酸化得到的含有羧基的G,由此推断F的结构简式为 ;(7)D的分子式为C9H11NO3,由于同分异构体的分子式相同,则H的分子式为C9H11NO3,H被酸性高锰酸钾溶液氧化为对苯二甲酸,说明H含有1个苯环、两个取代基位于苯环上的相对位置,且与苯环相连的碳上至少连有1个氢原子,最简单的α-氨基酸为氨基乙酸,则H的一个取代基为—CH(NH2)COOH,则另一个取代基为—CH2OH,所以H的结构简式为
;(7)D的分子式为C9H11NO3,由于同分异构体的分子式相同,则H的分子式为C9H11NO3,H被酸性高锰酸钾溶液氧化为对苯二甲酸,说明H含有1个苯环、两个取代基位于苯环上的相对位置,且与苯环相连的碳上至少连有1个氢原子,最简单的α-氨基酸为氨基乙酸,则H的一个取代基为—CH(NH2)COOH,则另一个取代基为—CH2OH,所以H的结构简式为 。
。
考点:考查有机合成和推断,涉及有机物的分子式、解释物质变化的原因、结构简式、化学方程式、同分异构体、官能团结构与性质等。


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:推断题
以乙烯为原料合成化合物C的流程如下所示:
(1) 乙醇和乙酸中所含官能团的名称分别为: 和 。
(2) B物质的结构简式为 。
(3) ① 、④的反应类型分别为 和 反应。
(4) 反应②和④的化学方程式分别为:
② ;
④ 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(16分)
有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
已知:
Ⅰ. (R、R`表示烃基)
(R、R`表示烃基)
Ⅱ.
(1)抗结肠炎药物有效成分分子中的含氧官能团名称是 。
(2)②中的反应条件是 ;G生成J的反应类型是 。
(3)①的化学方程式是 。
(4)F的结构简式是 。
(5)③的化学方程式是 。
(6)设计D→E和F→G两步反应的目的是 。
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式: 。
a.结构中有两个苯环,无其它环状结构 b.苯环上的一硝基取代产物有两种
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
贝诺酯是由扑热息痛、阿司匹林经化学法拼合制备的解热镇痛抗炎药,其合成如下(反应条件略去):
(1)扑热息痛的分子式是_________________
(2)下列叙述正确的是___________________
| A.生成贝诺酯的反应属于取代反应 |
| B.FeCl3溶液可区别阿司匹林和扑热息痛 |
| C.常温下贝诺酯在水中的溶解度小于扑热息痛 |
| D.贝诺酯既是酯类物质,也是氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15︰2︰8,其中化合物A的质谱图如下。
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1︰1︰2,它能够发生银镜反应。B为五元环酯。C的红外光谱表明其分子中存在甲基。其它物质的转化关系如下:
(1)I的分子式是: 。I分子中的官能团名称是: 。
(2)D和H的结构简式分别是: 、 。
(3)写出下列反应方程式(有机物用结构简式表示)
D→C ;
H→G 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
碱式碳酸铜和氯气都是用途广泛的化工原料。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl?)制备碱式碳酸铜,其制备过程如下:
已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |

查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高二上第一次月考化学试卷(解析版) 题型:选择题
T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )

A.在t1min时,3V正(B)=2V逆(C)
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动
C.T℃时,在相同容器中,若由0.3mol·L—1 A、0.1 mol·L—1 B和0.4 mol·L—1 C反应,达到平衡后,C的浓度仍为0.4 mol·L—1
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高一上学期第一次月考化学试卷(解析版) 题型:计算题
(10分)常温下,在27.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21g /cm3,求:
⑴ 该溶液中阴阳离子的总物质的量 .
⑵ 该溶液中CuSO4的物质的量浓度
⑶ 取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高二第一学期期中考试化学试卷(解析版) 题型:选择题
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是
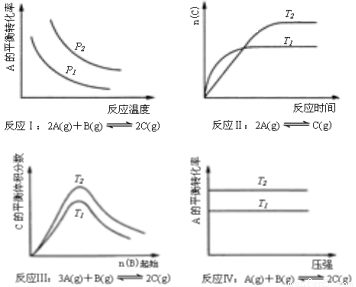
A.反应Ⅰ:△H>0,P2>P1 B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H>0,T2<T1 D.反应Ⅳ:△H<0,T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com