
| A、58.5g氯化钠固体中含有NA个氯化钠分子 |
| B、5.6 g铁粉与酸反应失去的电子数一定为0.2NA |
| C、6.0g金刚石中含有的共价键数为NA |
| D、标况下,11.2LSO3所含的分子数为0.5NA |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
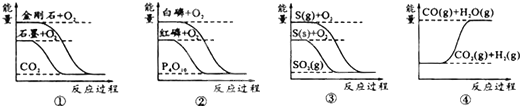
| A、石墨转变为金刚石是吸热反应 |
| B、白磷比红磷稳定 |
| C、CO (g)+H2O (g)=CO2 (g)+H2 (g)△H<0 |
| D、S (g)+O2 (g)=SO2 (g)△H1; S (s)+O2 (g)=SO2 (g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol 个氢气分子 |
| B、6.02×1023个氢气分子 |
| C、3.01×1023个氢气分子 |
| D、3.01×1023个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Mx |
| VNA |
| A、V L该气体的质量(以g为单位) |
| B、1 L该气体的质量(以g为单位) |
| C、1 mol该气体的体积(以L为单位) |
| D、1 L该气体中所含的分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、lmol FeI2与足量氯气反应时转移的电子数为2NA | ||
B、室温下,14.0g分子通式为CnH2n烯烃中含有的碳碳双键数目为
| ||
| C、标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | ||
| D、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| B、过量CO2通入NaOH溶液中:CO2+2OH-=CO32-+H2O |
| C、钠与水反应:2Na+2H2O=2Na++2OHˉ+H2↑ |
| D、稀硫酸中滴加氢氧化钡溶液:H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图(图中有部分仪器未画出),有一容积为300ml的注射器,与一500ml的蒸馏烧瓶相连,烧瓶中有0.384g铜片.现向烧瓶中加入18mL2.5mol.L-1的HNO3溶液,并立即用锡箔包住的橡皮塞封住瓶口.试回答:
如图(图中有部分仪器未画出),有一容积为300ml的注射器,与一500ml的蒸馏烧瓶相连,烧瓶中有0.384g铜片.现向烧瓶中加入18mL2.5mol.L-1的HNO3溶液,并立即用锡箔包住的橡皮塞封住瓶口.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com