
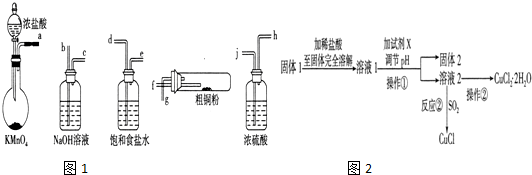
���� I��ʵ�������Դ�ͭ��������Fe��Ϊԭ���Ʊ�ͭ���Ȼ��Ũ���������ط�����Ӧ���������������л����Ȼ����ˮ�����ñ���ʳ��ˮ��ȥ�Ȼ��⣬��Ũ����������ʱӲ���Թ���ͭ��������Ӧ�����Ȼ�ͭ��������������Һ����������
��ͭ��������Fe����������Ӧ�����Ȼ������Ȼ�ͭ����ϡ�����ܽ⣬�γ��Ȼ������Ȼ�ͭ��Һ���ټ�CuO��������ͭ�ȵ���pH��ʹ������ת��Ϊ�����������������˵õ��Ĺ���2Ϊ������������Һ2Ϊ�Ȼ�ͭ��Һ��ͨ�����������������ͭ���ӷ���������ԭ��Ӧ����CuCl���Ȼ�ͭ��Һ��HCl��Χ�������ᾧ�õ�CuCl2•2H2O���Դ˽����⣮
��� �⣺I����1����������˳��Cl2����װ�á���ȥHCl����װ�á�����װ�á��Ʊ�װ�á�����Cl2����װ�ã����Ը������ӿ�˳���ǣ�a��d��e��j��h��f��g��b����ʵ�������ж�����μӷ�Ӧ������ʵ��ǰҪ����װ�õ������ԣ�
�ʴ�Ϊ��d��e��j��h��f��g��b��
��2��Ӳ���Թ��з�����Ӧ�У�������Cu��Ӧ�����Ȼ�ͭ����Fe��Ӧ�����Ȼ�������Ӧ����ʽ�ֱ�Ϊ��Cu+Cl2$\frac{\underline{\;\;��\;\;}}{\;}$CuCl2��2Fe+3Cl2$\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3��
�ʴ�Ϊ��Cu+Cl2$\frac{\underline{\;\;��\;\;}}{\;}$CuCl2��2Fe+3Cl2$\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3��
��3��������ͼ������֪��Һ2��������������������Fe3+����KSCN��Һ����Fe3+������Fe3+����Һ��죻
�ʴ�Ϊ��KSCN��Һ��
��4�����ڵ���pH�Գ�ȥ��Һ1���ʿɼ��Լ��������ᷴӦ���Ҳ�����Cu2+֮������ӣ�����CuO��Cu2��OH����Cu2��OH��2CO3��
�ʴ�Ϊ��c��e��
��5��������Ϣ��֪���ڼ��������£�SO2��ͭ���ӷ�Ӧ����CuCl��ɫ������SO42-���䷴Ӧ�����ӷ���ʽΪ��2Cu2++2Cl-+SO2+2H2O$\frac{\underline{\;\;��\;\;}}{\;}$2CuCl��+4H++SO42-��
�ʴ�Ϊ��2Cu2++2Cl-+SO2+2H2O$\frac{\underline{\;\;��\;\;}}{\;}$2CuCl��+4H++SO42-��
���� ���⿼�����ʵ��Ʊ�ʵ�鷽������ѧ�������̣�Ϊ�߿��������ͣ�������װ�ü������ķ������ۡ����Ӽ��顢���ӷ���ʽ����д�ȣ������ڻ���֪ʶ���ۺ�Ӧ�ã��Ѷ��еȣ�


 ����5��2���ϵ�д�
����5��2���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| X | ||
| Z |
| A�� | ԭ�Ӱ뾶��r��Y����r ��Z����r ��W�� | |
| B�� | Y��Z��W�ļ����ӵĵ��Ӳ�ṹ��ͬ | |
| C�� | XWm��YWn�л�ѧ��������ͬ��m��nΪ�������� | |
| D�� | Ԫ��Z �ļ���̬�⻯������ȶ��Ա�W ��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
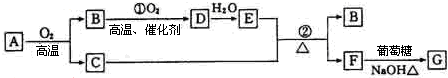
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
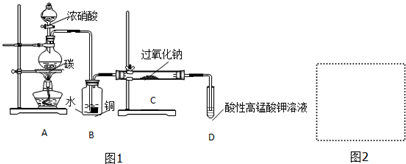
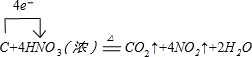
| ����� | 1 | 2 | 3 | 4 |
| KMnO4��Һ���/mL | 20.60 | 20.02 | 20.00 | 19.98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
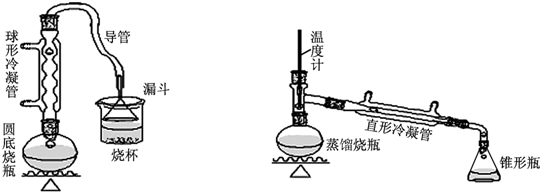
| ���� | �۵�/�� | �е�/�� |
| 1-���� | -89.5 | 117.3 |
| 1-�嶡�� | -112.4 | 101.6 |
| ���� | -95.3 | 142.4 |
| 1-��ϩ | -185.3 | -6.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
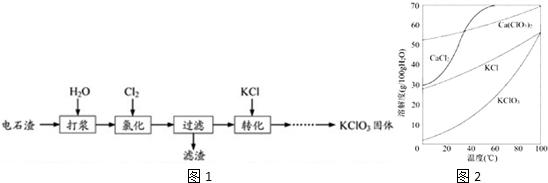
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ճ���������;��㡢�������Ľ������ϣ�
�����ճ���������;��㡢�������Ľ������ϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ܢݢޢ� | C�� | �ڢ� | D�� | �٢ڢۢܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
�� ��
���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com