
【题目】某学生为了探究浓硫酸的性质,实验过程及现象如下:向蔗糖中加入浓硫酸时,蔗糖变黑,体积膨胀,变成多孔的海绵状的炭,并放出有刺激性气味气体。该同学在实验中未涉及的浓硫酸性质是:
A. 吸水性 B. 脱水性 C. 酸性 D. 强氧化性
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 发生化学反应时,失去电子越多的金属原子,其还原能力越强
B. 目前已发现113种元素,即已发现113种原子
C. 核外电子总数不同的原子,可能是同种元素的原子
D. 同一元素的各种同位素的化学性质基本相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为延长舰船服役寿命可采用的电化学防腐的方法有①舰体与直流电源相连②舰体上镶嵌某种金属块。下列有关说法正确的是()
A. 方法①中舰体应连电源的正极 B. 方法②中镶嵌金属块可以是锌
C. 方法①为牺牲阳极的阴极保护法 D. 方法②为外加电流的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. SiO2、NO、SO2、SO3属于非金属氧化物,又属于酸性氧化物
B. NH3形成铵盐的过程属于氮的固定
C. 纯铁的熔点比生铁低
D. 可以用光洁无锈的铁丝代替铂丝作焰色反应实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)目前工业上有一种方法是用CO,和H2在230℃,催化剂条件下转化生成甲醇蒸汽和水蒸气。
图一表示恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图。写出该反应的热化学方程式_____________。
(2) “亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入(NH4)2SO4溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图二所示。

请写出a点时n(HSO3-):n(H2SO3)=______,b点时溶液pH=7,则n(NH4+):n(HSO3-)=___。
(3)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO![]() 5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图三所示:
5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图三所示:
① 请写出N2的电子式________。
② 曲线c对应NH3与NO的物质的量之比是______。
③ 曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为_____mg/(m3·s)。
(4)间接电化学法可除NO。其原理如图四所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性):_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2SO3溶液,可再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。下列说法正确的是
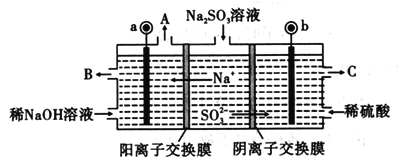
A. 电解过程中若消耗12.6gNa2SO3,则阴极区变化的质量为4.4g (假设该过程中所有液体进出口密闭)
B. b放电的电极反应式为SO32-+H2O-e-= SO42-+2H+
C. 电子由a经内电路流向b电极
D. 图中b极连接电源的正极,C 口流出的物质是亚硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A、B同主族, B、C、D.E同周期,B的核外电子数为C的1/2,D的最外层电子数为C、E之和的一半。 下列说法正确的是
A. A、B能形成离子化合物,且A离子半径小于B离子半径
B. A、D能形成离子化合物DA5,与水反应可产生两种气体
C. C、D的简单氢化物中只有D溶于水,其水溶液呈酸性
D. E形成的两种氢化物中所有化学键种类完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com