
【题目】2016年,美国研究小组开发出一种以糖为能源,可循环使用的环保电池装置。其工作原理如图所示。下列说法错误的是
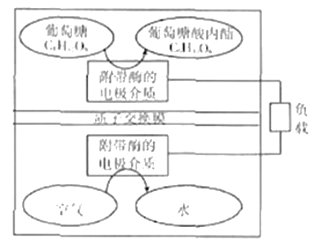
A. 葡萄糖在电池负极发生反应
B. 装置所示原理可以在强碱性条件下进行
C. 装置正极电极反应式为:O2+4e-+4H+=2H2O
D. 装置工作时,每消耗180g葡萄糖,将有2mol质子通过交换膜
【答案】B
【解析】A、该电池的总反应可以描述为:葡萄糖+O2→葡萄糖酸内酯+H2O,因此反应过程中葡萄糖被氧化,在原电池的负极参加反应,A正确。B、葡萄糖转变成葡萄糖酸内酯的过程需要“附带酶的电极介质”,而酶在强碱条件下会发生变性而失去活性,所以不宜在强酸、强碱等条件下进行,B错误。C、电池正负极间以质子交换膜分隔开,所以两极反应与质子(H+)有关,因此正极O2反应生成H2O的反应原理为:O2+4e-+4H+=2H2O,C正确。D、葡萄糖酸内酯结构是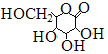 ,负极反应为:C6H12O6-2e-=C6H10O6+2H+,180g葡萄糖为
,负极反应为:C6H12O6-2e-=C6H10O6+2H+,180g葡萄糖为![]() ,则反应转移电子2 mol,D正确。所以错误答案选B。
,则反应转移电子2 mol,D正确。所以错误答案选B。


科目:高中化学 来源: 题型:
【题目】在NaCN溶液中存在水解平衡:CN-+H2O![]() HCN+OH-,水解常数
HCN+OH-,水解常数![]() [co(NaCN)是NaCN溶液的起始浓度]。25℃向1mol/L的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[p0H=-lgc(0H-)]的关系下图所示,下列说法错误的是
[co(NaCN)是NaCN溶液的起始浓度]。25℃向1mol/L的NaCN溶液中不断加水稀释,NaCN溶液浓度的对数值lgc0与2pOH[p0H=-lgc(0H-)]的关系下图所示,下列说法错误的是

A. 25℃时,Kn(CN-)的值为10-4.7
B. 升高温度,可使曲线上a点变到b点
C. 25℃,向a点对应的溶液中加入固体NaCN,CN-的水解程度减小
D. c点对应溶液中的c(OH-)大于a点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是
A. 常温常压下,11.2LO3所含的原子数为1.5NA
B. 常温常压下,18gH2O所含的分子数为NA
C. 标准状况下,16gO2所含的原子数为6NA
D. 标准状况下,11.2L氢气和氦气的混合气体所含的原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知几种难溶电解质的溶度积如下表所示:
几种难溶电解质的Ksp(25℃) | |
沉淀溶解平衡 | Ksp |
AgBr(s) | 5,0×10-13 mol2·L-2 |
AgI(s) | 8.3×10-17 mol2·L-2 |
FeS(s) | 6.3×10-18 mol2·L-2 |
ZnS(s) | 1.6×10-24 mol2·L-2 |
CuS(s) | 1.3×10-36 mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺为:____________________。
(2)向饱和的AgI溶液中加入固体硝酸银,则c( I- )________(填“增大”、“减小”或“不变”),若改加AgBr固体,则c(Ag+)__________(填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是_____________________(用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡: ZnS(s)![]() Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
A.加入少量CuS固体 B.加入少量FeS固体
C.加入少量FeCl2固体 D.加入少量CuCl2固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子的结构如图所示,下列说法正确的是( )

A.N4属于一种新型的化合物
B.N4与N2的摩尔质量相等
C.等质量的N4与N2所含的原子个数比为1∶1
D.等质量的N4与N2所含的原子个数比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列事实不能用勒夏特列原理解释的是 ( )
A.合成氨工业上增大压强以提高反应物的转化率
B.黄绿色的氯水光照后颜色变浅
C.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
D.在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺(CH3NH2)是一种应用广泛的一元弱碱。常温下,向200mL0.10mol/L的甲胺溶液中滴加V mL.0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是

A. b点对应加入盐酸的体积V< 20.00mL
B. 甲胺在水中的电离方程式为:CH3NH2+H2O![]() CH3NH3++OH-
CH3NH3++OH-
C. 常温下,甲胺的电离常数为Kb,则pKb=-1gKb=4.3
D. c点可能存在关系: 2c(H+)+ c(CH3NH3+)=c(CH3NH2) +2c(OH- )+ c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
B. NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
C. Cu2(OH)2CO3![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2
D. SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO4
(NH4)2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com