
下列物质中:①Mg ②液态氯化氢 ③干冰 ④食盐水 ⑤BaSO4 ⑥熔融氢氧化钠⑦稀硫酸 ⑧冰醋酸  ⑨乙醇 ⑩固体氯化钠
⑨乙醇 ⑩固体氯化钠
其中(1)属于电解质的是______ __;
(2)属于非电解质的是_____ ___;
(3)能导电的是____ ____。
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:实验题
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42﹣ HCO3﹣ NO3﹣ OH﹣ |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E 溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B ,D 。
(2)将含1mol A的溶液与含1m ol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
ol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
(3)在A溶液中加少入量澄清石灰水,其离子方程式为 。
(4)C常用作净水剂,用离子方程式表示其净水原理 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
在无水栽培中,需配制一种含有50molNH4Cl、16molKCl和24molK2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,其物质的量分别为
A.2mol、64mol、24mol B.64mol、2mol、24mol
C.32mol、50mol、12mol D.16mol、50mol、24mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列说法正确的是
A.在常温常压下,11.2 LN2含有的分子数为0.5 NA
B.71gCl2所含原子数为NA
C.在常温常压下,1molNe含有的原子数为NA
D.在同温、同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:填空题
研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单的理解为断开1 mol 化学键时所需吸收的能量。下表是部分化学键的键能数据:
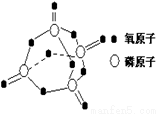
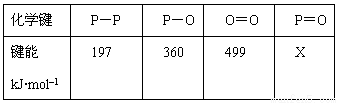
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图所示,则上表中X= kJ·mol–1。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡常数减小 | B. | 物质A的转化率增加了 | ||
| C. | 平衡向逆反应方向移动了 | D. | a>b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com