
【题目】高锰酸钾是中学常用化学试剂,工业上常以软锰矿(主要成分是MnO2)为原料进行制备,主要工艺流程如下图:

已知:3K2MnO4+2H3PO4═2KMnO4+MnO2↓+2K2HPO4+2H2O
物质 | KMnO4 | K2HPO4 | K2SO4 | CH3COOK | KCl | K2CO3 |
293K溶解度/g | 6.4 | 150 | 11.1 | 217 | 34 | 111 |
(1)原料高温煅烧时选用铁坩埚和铁棒,理由是__________。
(2)①中每生成1molK2MnO4时电子转移2mol,写出化学反应方程式_________。
(3)从反应机理和产物分离角度考虑,③可用磷酸,也可用下列________试剂。
A.醋酸 B.盐酸 C.硫酸 D.CO2
(4)下列描述不正确的是_________。
A.操作⑤中蒸发至大量晶体析出再冷却晶体,趁热过滤
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸
C.可用无水乙醇洗涤产品提高纯度
D.KMnO4晶体的烘干温度过高会降低产率
(5)粗产品的洗涤步骤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复2~3次。
请选出正确的操作并排序________。(操作可重复使用)
(6)高锰酸钾产品的纯度测定:准确称取0.7900g产品,配成250mL溶液,量取25.00mL于锥形瓶中,用0.1000molL﹣1(NH4)2Fe(SO4)2标准溶液进行滴定,滴定终点的现象__________。滴定前和滴定后的液面见下图。计算出高锰酸钾的纯度为_______。

【答案】高温下瓷坩埚和玻璃棒会与KOH等反应,与铁不反应 6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O AD ABC dabef 滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色 88.00%
3K2MnO4 +KCl+3H2O AD ABC dabef 滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色 88.00%
【解析】
(1)高温下瓷坩埚和玻璃棒中的二氧化硅和KOH等反应,被腐蚀,而铁坩埚和铁棒不反应。
(2)①中每生成1molK2MnO4时电子转移2mol,则生成3molK2MnO4时电子转移6mol;每1molKClO3参加反应转移电子6mol,根得失电子守恒,则KClO3与K2MnO4的物质的量比为1:3,则此反应的化学反应方程式为6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O。(3)根据表格中的数据CH3COOK和 K2CO3的溶解度比KMnO4大的多,蒸发浓缩基本上会留在母液中,其它的溶解度和KMnO4接近,会随KMnO4结晶析出。故BC不符合题意,AD符合题意。答案选AD。
3K2MnO4 +KCl+3H2O。(3)根据表格中的数据CH3COOK和 K2CO3的溶解度比KMnO4大的多,蒸发浓缩基本上会留在母液中,其它的溶解度和KMnO4接近,会随KMnO4结晶析出。故BC不符合题意,AD符合题意。答案选AD。
(4)A.操作⑤中蒸发至大量晶体析出,趁热过滤,防止出现大量的副产品,故A错误;
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸,故B正确。
C.不能用无水乙醇洗涤产品提高纯度,无水乙醇会与高锰酸钾反应,被高锰酸钾氧化,故C错误;
D.KMnO4受热易分解,KMnO4晶体的烘干温度过高会降低产率,应低温烘干,故D正确。(5)粗产品的洗涤步骤应为dabef的顺序排列。(6)高锰酸钾会与(NH4)2Fe(SO4)2发生氧化还原反应,当恰好反应时,高锰酸钾紫色刚好褪去,则滴定终点的现象为滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色;由图滴定前和滴定后的液面可知,滴定过程中消耗(NH4)2Fe(SO4)2溶液的体积为22.00mL。滴定过程中高锰酸钾和(NH4)2Fe(SO4)2发生氧化还原反应,高锰酸钾中锰元素价态由+7价降低到+2价生成Mn2+,(NH4)2Fe(SO4)2中Fe2+由+2价升高到+3价生成Fe3+,根据化合价升降守恒,高锰酸钾和(NH4)2Fe(SO4)2的物质的量比为1:5时恰好反应。过程中消耗n[(NH4)2Fe(SO4)2]=0.022L×0.1000molL﹣1=0.0022mol,则锥形瓶中25.00mL的高锰酸钾的物质的量为n(KMnO4)=0.0022mol÷5=0.00044mol,则250.00mL的高锰酸钾的物质的量0.0044mol,质量为m(KMnO4)=0.0044mol×158g/mol=0.6952g,则高锰酸钾的纯度为0.06952÷0.7900×100%=88.00%。
(1)高温下瓷坩埚和玻璃棒中的二氧化硅和KOH等反应,被腐蚀,而铁坩埚和铁棒不反应。本小题答案为:高温下瓷坩埚和玻璃棒会与KOH等反应,与铁不反应。
(2)①中每生成1molK2MnO4时电子转移2mol,则生成3molK2MnO4时电子转移6mol;每1molKClO3参加反应转移电子6mol,根得失电子守恒,则KClO3与K2MnO4的物质的量比为1:3,则此反应的化学反应方程式为6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O。本小题答案为:6KOH+KClO3+3MnO2
3K2MnO4 +KCl+3H2O。本小题答案为:6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O。
3K2MnO4 +KCl+3H2O。
(3)根据表格中数据CH3COOK和 K2CO3的溶解度比KMnO4大的多,蒸发浓缩基本上会留在母液中,其它的溶解度和KMnO4接近,会随KMnO4结晶析出。故BC不符合题意,AD符合题意。答案选AD。
(4)A.操作⑤中蒸发至大量晶体析出,趁热过滤,防止出现大量的副产品,故A错误;
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸,故B正确。
C.不能用无水乙醇洗涤产品提高纯度,无水乙醇会与高锰酸钾反应,被高锰酸钾氧化,故C错误;
D.KMnO4受热易分解,KMnO4晶体的烘干温度过高会降低产率,应低温烘干,故D正确。答案选AC。
(5)粗产品的洗涤步骤应为dabef的顺序排列。本小题答案为:dabef。
(6)高锰酸钾会与(NH4)2Fe(SOspan>4)2发生氧化还原反应,当恰好反应时,高锰酸钾紫色刚好褪去,则滴定终点的现象为滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色;由图滴定前和滴定后的液面可知,滴定过程中消耗(NH4)2Fe(SO4)2溶液的体积为22.00mL。滴定过程中高锰酸钾和(NH4)2Fe(SO4)2发生氧化还原反应,高锰酸钾中锰元素价态由+7价降低到+2价生成Mn2+,(NH4)2Fe(SO4)2中Fe2+由+2价升高到+3价生成Fe3+,根据化合价升降守恒,高锰酸钾和(NH4)2Fe(SO4)2的物质的量比为1:5时恰好反应。过程中消耗n[(NH4)2Fe(SO4)2]=0.022L×0.1000molL﹣1=0.0022mol,则锥形瓶中25.00mL的高锰酸钾的物质的量为n(KMnO4)=0.0022mol÷5=0.00044mol,则250.00mL的高锰酸钾的物质的量0.0044mol,质量为m(KMnO4)=0.0044mol×158g/mol=0.6952g,则高锰酸钾的纯度为0.06952÷0.7900×100%=88.00%。本小题答案为:滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色;88.00%。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:

①装置D的名称为___________。
②按照气流从左到右的方向,上述装置的连接顺序为___________→尾气处理装置(填仪器接口的字母编号)。
③实验前先通入一段时间N2,其目的为______________________。
④实验证明了气体产物中含有CO,依据的实验现象为______________________。
(2)固体产物成分的探究。充分反应后,A处反应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为___________。
(3)依据(1)和(2)结论,可知A处反应管中发生反应的化学方程式为___________。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液。
步骤2:取上述溶液25.00mL,用c mol· L -1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤3中加入锌粉的目的为____________________________________________。
(5)草酸亚铁晶体样品的纯度为____________________________________________;若步骤1配制溶液时部分Fe2+被氧化,则测定结果将___________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表是某位生物教师的肝肾糖脂血液化验单部分内容:
已知:1摩尔(mol)等于1000毫摩尔(mmol),血液中葡萄糖简称血糖,分子式为C6H12O6,请根据以上信息回答下列问题:
项目名称 | 数据 | 参考值 |
尿素氮 | 2.95 | 2.00﹣6.10mmol.L﹣1 |
葡萄糖 | 4.50 | 3.89﹣6.11mmol.L﹣1 |
总胆固醇 | 3.75 | <5.20mmol.L﹣1 |
甘油三酯 | 1.80↑ | <1.70mmol.L﹣1 |
(1)这位教师的血糖含量属___(填“正常”、“偏高”或“偏低”)。
(2)这位教师的1mL血液中含葡萄糖___g。
Ⅱ.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。表是500mL“鲜花保鲜剂”中含有的成分,阅读并回答下列问题:
成分 | 成分的质量(g) | 摩尔质量(gmol﹣1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.02 | 170 |
(1)下列“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为___。
(2)配制上述“鲜花保鲜剂”所的仪器有烧杯、玻璃棒、药匙、托盘天平(带砝码)、___(填所缺仪器的名称)。
(3)若要配制0.5mol/L500mL的硫酸溶液,现有质量分数为98%、密度为1.84g·cm﹣3的浓硫酸。实验室有15mL、20mL、50mL量筒,应选用___mL量筒最好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O IO![]() →I2 MnO
→I2 MnO![]() →Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
→Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A. H2O2 B. HNO2 C. MnO![]() D. IO
D. IO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目。____________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______,MnO![]() +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B. 除短周期外,其他周期均有18种元素
C. 副族元素中没有非金属元素
D. 碱金属元素是指ⅠA族的所有元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A. 已知2SO2(g)+O2 ![]() 2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
B. 已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C. 已知H+(aq)+OH-(aq)=H2O(1),△H=-57.3kJ/mol,则任何酸碱中和反应的热效应均为57.3 kJ
D. 已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2 则△H1<△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,烧杯中的溶液为2 mol·L-1CH3COOH溶液,接通直流电源。分别向烧杯中加入下列物质(保持反应温度不变),灯泡变暗的是( )

A.加入固体NaOHB.加水稀释C.加入金属NaD.通入HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是中学常用化学试剂,工业上常以软锰矿(主要成分是MnO2)为原料进行制备,主要工艺流程如下图:
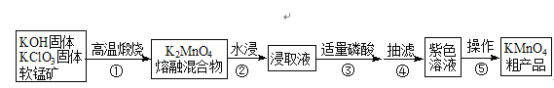
已知:3K2MnO4+2H3PO4═2KMnO4+MnO2↓+2K2HPO4+2H2O
物质 | KMnO4 | K2HPO4 | K2SO4 | CH3COOK | KCl | K2CO3 |
293K溶解度/g | 6.4 | 150 | 11.1 | 217 | 34 | 111 |
(1)原料高温煅烧时选用铁坩埚和铁棒,理由是__________。
(2)①中每生成1molK2MnO4时电子转移2mol,写出化学反应方程式_________。
(3)从反应机理和产物分离角度考虑,③可用磷酸,也可用下列________试剂。
A.醋酸 B.盐酸 C.硫酸 D.CO2
(4)下列描述不正确的是_________。
A.操作⑤中蒸发至大量晶体析出再冷却晶体,趁热过滤
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸
C.可用无水乙醇洗涤产品提高纯度
D.KMnO4晶体的烘干温度过高会降低产率
(5)粗产品的洗涤步骤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复2~3次。
请选出正确的操作并排序________。(操作可重复使用)
(6)高锰酸钾产品的纯度测定:准确称取0.7900g产品,配成250mL溶液,量取25.00mL于锥形瓶中,用0.1000molL﹣1(NH4)2Fe(SO4)2标准溶液进行滴定,滴定终点的现象__________。滴定前和滴定后的液面见下图。计算出高锰酸钾的纯度为_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com