
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目。____________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______,MnO![]() +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
【答案】C K2S和N2 +1 CuI 0.5 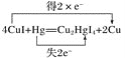 1 5 8 1 5 4 0.007
1 5 8 1 5 4 0.007
【解析】
(1)氧化还原反应反应中,氧化剂中元素的化合价降低,发生还原反应,对应产物为还原产物;还原剂中元素化合价升高,发生氧化反应,对应产物为氧化产物;据以上分析解答。
(2)反应4CuI+Hg=Cu2HgI4+2Cu中,铜元素的化合价由+1价降到0价,所以CuI做氧化剂;汞元素的化合价由0价升高到+2价,汞做还原剂;该反应共转移2e-电子,据此标出电子转移的方向和数目,并根据2e--4CuI关系进行计算;
(3)①根据氧化还原反应中电子守恒、电荷守恒、原子守恒进行配平;
②设与(NH4)2Fe(SO4)2反应消耗高锰酸钾xmol,根据反应MnO4-+5Fe2++8H+===Mn2++5Fe3++4H2O列方程进行计算。
(1)本反应中,氮元素的化合价由+5价变为0价,硫元素的化合价由0价变为-2价,碳元素的化合价由0价变为+4价,被氧化的元素是C。氧化剂是KNO3和S,氧化产物是CO2,还原产物是K2S和N2。
综上所述,本题答案是:C,K2S和N2。
(2)①I元素的负价只有-1价,Cu在化合物中只有+1、+2价,再由化学式中各元素正负化合价代数和等于零确定各元素的化合价,由此可确定Cu2HgI4中Cu为+1价,Hg为+2价。
综上所述,本题答案是:+1。
②反应4CuI+Hg===Cu2HgI4+2Cu中,铜元素由+1价降到0价,发生还原反应,所以氧化剂为CuI;每4mol CuI参加反应转移电子2 mol,即当有1molCuI参加反应时,转移电子0.5 mol。
综上所述,本题答案是:CuI,0.5。
③反应4CuI+Hg===Cu2HgI4+2Cu中,1molHg参加反应转移电子2mol,所以该反应电子转移的方向和数目如下: ;
;
综上所述,本题答案是: 。
。
(3)①反应中Mn元素的化合价由+7降低到+2,Fe元素的化合价由+2升高到+3,由电子守恒、电荷守恒、原子守恒可知,离子反应为MnO4-+5Fe2++8H+===Mn2++5Fe3++4H2O。
综上所述,本题答案是:1 5 8 1 5 4。
②设与(NH4)2Fe(SO4)2反应消耗高锰酸钾xmol,则
MnO4-+5Fe2++8H+===Mn2++5Fe3++4H2O
1mol 5mol
xmol 0.350L×0.1mol·L-1
所以x=0.007,即与固体混合物反应后剩余KMnO4的物质的量为0.007 mol。
综上所述,本题答案是:0.007。


科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按如下图装置进行制取。
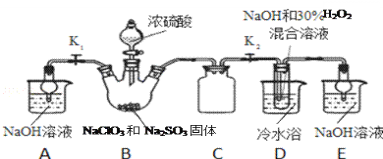
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)已知装置B中的产物有ClO2气体,则装置B中反应的化学方程式为___________;装置D中反应生成NaClO2的化学方程式为________________________;
(2)装置B中反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还肯定含有的一种阴离子是________________;检验该离子的方法是________________________;
(3)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②__________;③用38℃~60℃热水洗涤;④低于60℃干燥;得到成品。
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是________________________;
实验Ⅱ:样品杂质分析与纯度测定
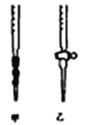
(5)测定样品中NaClO2的纯度.测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c molL﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL
①用Na2S2O3标准溶液滴定时,应将Na2S2O3标准溶液注入________(填“甲”或“乙”)中。
②观察Na2S2O3标准溶液滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致待测溶液浓度测定值___________(选填“偏大”“偏小”或“无影响”)。
③(已知:I2+2S2O32﹣=2I﹣+S4O62﹣)。请计算所称取的样品中NaClO2的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中是各组反应的反应物和反应温度,反应刚开始时,放出H2速率最快的是( )
编号 | 金属(粉末状) | 物质的量(mol) | 酸的浓度及体积 | 反应温度(℃) |
A | Al | 0.1 | 2mol.L-1盐酸10mL | 60 |
B | Fe | 0.1 | 1mol.L-1盐酸10mL | 50 |
C | Mg | 0.1 | 1mol.L-1盐酸10mL | 60 |
D | Mg | 0.1 | 1mol.L-1硫酸10mL | 60 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成气体(标准状况,下同)的体积为b L。反应的化学方程式是_________________________________________________________;样品中铝的质量是________ g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是__________________________________________________;氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于Fe+2HCl=FeCl2+ H2↑反应,下列说法不正确的是( )
A.Fe是还原剂,被氧化
B.HCl是氧化剂,发生了还原反应
C.-1价氯在反应中价态未变,所以HCl既不是氧化剂,又不是还原剂
D.此反应既是置换反应又是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。A是元素Y的单质。常温下,甲的浓溶液和A发生钝化。丙、丁、戊是由这些元素组成的二元化合物,且丙是无色气体。上述物质的转化关系如图所示。下列说法正确的是
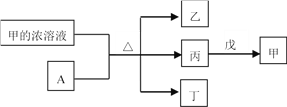
A. 丁和戊中所含元素种类相同
B. 简单离子半径大小:X<Y
C. 气态氢化物的还原性:X>Z
D. Y的简单离子与Z的简单离子在水溶液中可大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍。试回答:
(1)这四种元素分别是:A____,B___,C___,D____。
(2)这四种元素中在常温常压下的液态或气态氢化物的稳定性由大而小的顺序是_____。
(3)A与B形成的三原子分子的电子式是___,B与D形成原子个数比为1∶1的化合物的电子式是_____。
(4)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度下,向2m g 16%的CuSO4溶液中加入m g CuSO45H2O,溶液恰好达到饱和,该饱和溶液中CuSO4的质量分数为_____。
(2)标准状况下,1体积水可溶解V体积HCl气体,所得溶液的密度为ρg/cm3,则所得溶液溶质的质量分数表示为_____,溶质的物质的量浓度表示为_____。
(3)若以ω1和ω2分别表示浓度为a molL﹣1和b molL﹣1硫酸溶液的溶质的质量分数,且知 2a=b,则下列推断正确的是(硫酸溶液的密度比纯水的大)_____(填序号)
A. 2ω1=ω2 B. ω2<2ω1 C. ω2>2ω1 D. ω1<ω2<2ω1
(4)若以ω1和ω2分别表示浓度为a molL﹣1和b molL﹣1氨水的溶质的质量分数,且知2ω1=ω2,则下列推断正确的是(氨水的密度比纯水的小)_____(填序号)
A. 2a=b B. 2a<b C. 2a>b D. a<b<2a.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是425℃时,在1 L密闭容器中发生化学反应的浓度随时间的变化示意图。
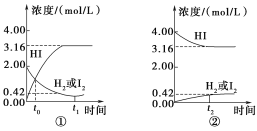
下列叙述错误的是( )
A. 图①中t0时,三种物质的物质的量相同
B. 图①中t0时,反应达到平衡状态
C. 图②中的可逆反应为2HI(g) ![]() H2(g)+I2(g)
H2(g)+I2(g)
D. 图①②中当c(HI)=3.16 mol/L时,反应达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com