

 2H2��+O2����֪������2molH2��ת��4mol���ӣ����Ե�������Ӧ��ת��0.5mol����ʱ�����ɵ�H2Ϊ0.25mol������µ����Ϊ0.25mol��22.4L/mol=5.6L��
2H2��+O2����֪������2molH2��ת��4mol���ӣ����Ե�������Ӧ��ת��0.5mol����ʱ�����ɵ�H2Ϊ0.25mol������µ����Ϊ0.25mol��22.4L/mol=5.6L��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ں����������п�鱣����Dz��ܸ�ʴ�Dz������������������������� |
| B������������Ʒ�ĶƲ�����ʱ���Ʋ����ܶ�����Ʒ�𱣻����� |
| C�������������ڿ�������绯ѧ��ʴ�����䰵 |
| D��������ʴ�ĵ绯ѧ��ʴ����������ԭ���ԭ������ԭ���ԭ���������ڽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����X-Y�Ͻ����ڳ�ʪ�����У�X�ȸ�ʴ |
| B��Xԭ��������������Yԭ�������������� |
| C��X�ܴ�Y������Һ�а�Y�û����� |
| D�����X��Y���εĻ����Һ��������������Y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��12��72% |
| B��7��96% |
| C��8��30% |
| D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��Fe ��3 ="=" ="="  | B��2H2O + O2 + 4 ==4OH�� ==4OH�� |
C��Fe ��2 ="=" ="=" 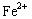 | D��4OH����4 ==2H2O + O2�� ==2H2O + O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Fe �C 2e- =" Fe2+" | B��2H+ + 2e- =" H2��" |
| C��2H2O + O2 + 4e- =" 4OH-" | D��4OH- - 4e- =" 2H2O" + O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ʴ���ǽ���ʧȥ���ӱ���ԭ�Ĺ��� |
| B����������Ľ��������ֱ����Դ�ĸ���������������������� |
| C����п��Ƥ������ʴʱ�������ĵ缫��ӦʽΪ��Fe-2e�� Fe2+ |
| D�������ڳ�ʪ���������⣬����Ϊֱ�ӷ�����Ӧ��4Fe+3O2��2Fe2O3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com