
下列说法正确的是
| A.往沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,可制得Fe(OH)3胶体 |
B.CO2溶于水中,只存在平衡:CO2+H2O H2CO3 H2CO3 |
| C.在潮湿的空气中,生铁比纯铁更耐腐蚀 |
| D.实验室可用浓H2SO4制备HCl,这是因为H2SO4的酸性比HCl强 |
A
解析试题分析:在沸水中加入几滴饱和氯化铁溶液,使氯化铁的水解平衡向生成氢氧化铁的方向移动,当溶液变为红褐色时,就制取了氢氧化铁胶体,故A正确;二氧化碳溶于水时,不仅存在二氧化碳的溶解平衡,还存在碳酸的电离平衡:H2CO3 H++HCO3-等,故B错误;生铁是Fe—C合金,在潮湿的空气中可形成原电池,铁作负极,发生吸氧腐蚀或析氢腐蚀,而纯铁不能形成原电池,所以生铁更容易腐蚀,故C错误;硫酸、氯化氢都能完全电离,都是强酸,实验室用浓硫酸制取氯化氢的原因是浓硫酸的沸点高于氯化氢,或者浓硫酸的挥发性小于氯化氢,故D错误。
H++HCO3-等,故B错误;生铁是Fe—C合金,在潮湿的空气中可形成原电池,铁作负极,发生吸氧腐蚀或析氢腐蚀,而纯铁不能形成原电池,所以生铁更容易腐蚀,故C错误;硫酸、氯化氢都能完全电离,都是强酸,实验室用浓硫酸制取氯化氢的原因是浓硫酸的沸点高于氯化氢,或者浓硫酸的挥发性小于氯化氢,故D错误。
考点:考查元素化合物的主要性质及制备,涉及氢氧化铁胶体的制取方法、二氧化碳溶于水后的化学平衡、生铁和纯铁的腐蚀、浓硫酸的难挥发性等。


科目:高中化学 来源: 题型:单选题
已知A 、B、C、D之间的转化关系如图所示。下列说法正确的是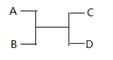
A.若A为Fe,D为氢气,则B一定为酸
B.若A、D为化合物,B为水,则C一定是气体单质
C.若A、B、C、D均为化合物,该反应一定属于复分解反应
D.若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关物质的性质及应用均正确的是 ( )
| A.常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B.氢氧化铁胶体具有很强的吸附性,可用于除去水中的所有杂质 |
| C.二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法不正确的是
| A.明矾净化水是因为明矾的水解产物有吸附作用 |
| B.FeCl3溶液腐蚀铜电路板的过程发生了置换反应 |
| C.氨氧化法制硝酸的过程中有NO2生成 |
| D.氯碱工业中,NaOH是在阴极室中产生的 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下列实验现象得出的结论,正确的是
| 选项 | 实验现象 | 结论 |
| A | 某气体能使润湿的淀粉碘化钾试纸变蓝 | 该气体一定是氯气 |
| B | 向某溶液中加入盐酸酸化的BaCl2,有白色沉淀生成 | 该溶液中一定存在SO42- |
| C | 铁与稀硝酸充分反应后,溶液呈浅绿色 | 稀硝酸与铁反应只能生成Fe2+ |
| D | SO2通入溴水中,溴水褪色 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列陈述I、II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | Fe2(SO4)3可以做净水剂 | Fe 3+水解成胶体可吸附水中的细小悬浮物 |
| B | 向Ba(NO3)2溶液中通入足量SO2,无明显现象 | 弱酸不能制强酸 |
| C | Cl2能使湿润的布条褪色 | Cl2具有漂白性 |
| D | 电解NaCl溶液制备金属钠 | NaCl是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关化学反应过程的叙述中,错误的是
| A.船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
| B.除去CO2中的少量SO2:通过盛有饱和NaHCO3溶液的洗气瓶 |
| C.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| D.金属钠在空气中燃烧产生黄色火焰,生成淡黄色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.硅和石墨都是重要的半导体材料 |
| B.SO2、NO2、CO2都会导致酸雨的形成 |
| C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理不同 |
| D.氢能是清洁能源,工业上用电解水法制大量氢气符合节能减排理念 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂
质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。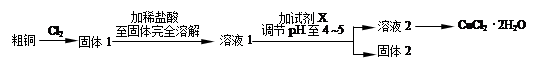
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
① 仪器A的名称是 。
② 装置B中发生反应的离子方程式是 。
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要
(填“是”或“否”) 。
(2)试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号) 。
a.NaOH b.NH3·H2O c.CuO d.Cu2(OH) 2CO3 e.CuSO4
(3)在溶液2转化为CuCl2·2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) +4Cl-(aq) CuCl42-(aq) +4H2O(l)
CuCl42-(aq) +4H2O(l)
蓝色 绿色
① 上述反应的化学平衡常数表达式是K= 。若增大氯离子浓度,K值(填“增大”、“减小”或“不变”) 。
② 取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号) 。
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com