
下列陈述I、II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | Fe2(SO4)3可以做净水剂 | Fe 3+水解成胶体可吸附水中的细小悬浮物 |
| B | 向Ba(NO3)2溶液中通入足量SO2,无明显现象 | 弱酸不能制强酸 |
| C | Cl2能使湿润的布条褪色 | Cl2具有漂白性 |
| D | 电解NaCl溶液制备金属钠 | NaCl是离子化合物 |
A
解析试题分析:硫酸铁是强酸弱碱盐,所含铁离子能水解,生成氢氧化铁胶体,氢氧化铁胶体具有很强的吸附性,可以将水中的细小悬浮物除去,因此硫酸铁可做净水剂,则陈述I、II均正确且有因果关系,故A正确;硝酸钡是硝酸盐,硝酸盐溶液具有氧化性,二氧化硫气体具有还原性,根据氧化还原反应中强制弱原理,向Ba(NO3)2溶液中通入足量SO2,生成硫酸钡沉淀、一氧化氮气体等,即Ba(NO3)2+ 3SO2+2H2O=BaSO4↓+2NO↑+2H2SO4,则陈述I、II均错,故B错;氯气与水发生氧化还原反应,生成盐酸和次氯酸,次氯酸具有强氧化性,具有漂白作者,能使布条褪色,虽然氯气也具有强氧化性,氮它没有漂白作用,则陈述I正确、II错,故C错;电解熔融氯化钠可以制备金属钠,因为氯化钠是离子化合物,电解氯化钠溶液不可能制备金属钠,因为溶液氢离子比钠离子容易得到电子,氢离子优先被还原为氢气,则陈述I错、陈述II正确,故D错。
考点:考查无机物的性质及应用,涉及铁离子的水解性及其应用、硝酸盐的氧化性及应用、二氧化硫气体的还原性及其应用、氯气的强氧化性及其应用、次氯酸的漂白作用、金属钠的制备原理、电解氯化钠溶液的原理等。


科目:高中化学 来源: 题型:单选题
右下图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出)。下列说法错误的是
| A.右图所示的反应均为氧化还原反应 |
| B.比较镁、铁与水的反应条件,可知铁的金属性比镁弱 |
| C.工业上常用NO2与水的反应原理制取硝酸 |
| D.实验室中可用铜与稀硝酸反应制取NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在化学学习与研究中类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中正确的是( )
①HCl气体可被浓硫酸干燥,HI气体也可被浓硫酸干燥,
②过量CO2通入漂白粉溶液,所得溶液具有漂白性,过量SO2通入漂白粉溶液,所得溶液也具有漂白性(不考虑溶解)
③苯不能使酸性高锰酸钾褪色,甲苯也不能使酸性高锰酸钾褪色
④Al(OH)3.Cu(OH)2受热易分解,Fe(OH)3受热也易分解
⑤37℃时,Fe3+.Cu2+能催化H2O2的分解;100℃时,MnO2.过氧化氢酶也能催化H2O2的分解
| A.④ | B.②③ | C.④⑤ | D.①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 把SO2通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
| B | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
| C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变浅 | 反应2NO2 N2O4的△H<0 N2O4的△H<0 |
| D | 向AgCl沉淀中滴加KI溶液 | 白色沉淀变为黄色 | 溶度积:AgI比AgCl更小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.往沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,可制得Fe(OH)3胶体 |
B.CO2溶于水中,只存在平衡:CO2+H2O H2CO3 H2CO3 |
| C.在潮湿的空气中,生铁比纯铁更耐腐蚀 |
| D.实验室可用浓H2SO4制备HCl,这是因为H2SO4的酸性比HCl强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用4种溶液进行实验,下表中“试剂和操作”与“现象”对应关系正确的是
| 选项 | 试剂和操作 | 现象 |
| A | 向AlCl3溶液中滴入过量的氨水 | 溶液先有白色沉淀,后来沉淀消失 |
| B | 向新生成的AgC1浊液中滴入KI溶液,振荡 | 白色沉淀逐渐转化为黄色沉淀 |
| C | 向Ca(C1O)2溶液中先通入CO2,再加入少量品红溶液 | 溶液先变浑浊,通入CO2后品红的红色不褪去 |
| D | 向BaC12溶液中先通入SO2,再通入过量NO2 | 先生成沉淀,后来沉淀消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向100mL18mol/L的硫酸中加入足量铜片,加热并充分反应。下列有关说法正确的是
| A.充分反应后转移1.8mol电子 | B.H2SO4只作氧化剂 |
| C.若不加热应生成H2 | D.消耗的铜的质量一定少于57.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 LH2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
(1)甲的化学式是_________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________________________________。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式_________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之______________。(已知Cu2O+2H+==Cu+Cu2++H2O)
(5)甲与乙之间_______(填“可能”或“不可能”)发生反应产生H2,判断理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题: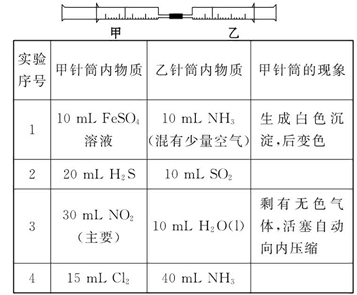
(1)实验1中,沉淀最终变为_______色,写出沉淀变色的化学方程式_____________________。
(2)实验2甲针筒内的现象是:有_______生成,甲筒活塞_______移动(填“向外”、“向内”或“不”)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入_______溶液中。
(3)实验3中,甲中的30 mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是_______,写出NO2与H2O反应的化学方程式____________________________。
(4)实验4中,已知:3Cl2+2NH3=N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为_______。最后针筒内剩余气体的体积约为_______mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com