
【题目】下列物质中既有离子键又有共价键的是
A.NaOHB.H2OC.K2OD.CaCl2
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.铜丝能导电,所以铜是电解质
B.固体氯化钠不导电,所以氯化钠不是电解质
C.SO3溶于水能导电,所以SO3是电解质
D.氯化氢水溶液能导电,所以氯化氢是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点A2D<A2X
B. CA3分子是非极性分子
C. C形成的单质中σ键与π键个数之比为1∶2
D. B、C、D形成的气态氢化物互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.2 mol·L-1NaOH溶液480 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。

(2)下列有关容量瓶使用方法的操作中,错误的是_______。
A.使用容量瓶之前应检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒,摇匀
(3)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为________g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________(填“>”“<”或“=”)0.2 mol·L-1;
③若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度________(填“>”“<”或“=”)0.2 mol·L-1。
(4)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________(计算结果保留一位小数)mL;
②如果实验室有15 mL、20 mL、50 mL量筒,应选用______mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是___________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员在探究如何降低大气中氮氧化物与碳氧化物的含量方面做出了巨大贡献,并取得了显著的成绩。
(1)反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H<0,可用于净化汽车尾气,已知570K时该反应的反应速率极慢,平衡常数极大。提高尾气净化效率的最佳途径是下列措施中的______(填标号);若要净化汽车尾气的同时提高该反应的速率和NO的平衡转化率,且只改变一个反应条件,则应采取的措施是____(填标号)。
2CO2(g)+N2(g) △H<0,可用于净化汽车尾气,已知570K时该反应的反应速率极慢,平衡常数极大。提高尾气净化效率的最佳途径是下列措施中的______(填标号);若要净化汽车尾气的同时提高该反应的速率和NO的平衡转化率,且只改变一个反应条件,则应采取的措施是____(填标号)。
a.研制、使用高效催化剂 b.升高温度
c.增大压强 d.用碱溶液吸收CO2
(2)已知:△H=产物的总摩尔生成焓-反应物的总摩尔生成焓。25℃,101kPa时,NO、CO、CO2、N2的摩尔生成焓分别为+90.3kJ·mol-1、-110.5kJ·mol-1、-393.5kJ·mol-1、0 kJ·mol-1,则2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)的△H=___________________。
2CO2(g)+N2(g)的△H=___________________。
(3)某科研小组根据反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)来探究反应物起始时的碳氮比
2CO2(g)+N2(g)来探究反应物起始时的碳氮比![]() 对污染物去除率的影响。T℃时,向体积为1L的恒容密闭容器中充入总物质的量为4mol的NO和CO混合气体,并加入一定量的固体催化剂进行反应,实验测得平衡体系中气体组分转化率和氮气的体积分数的变化如图所示。
对污染物去除率的影响。T℃时,向体积为1L的恒容密闭容器中充入总物质的量为4mol的NO和CO混合气体,并加入一定量的固体催化剂进行反应,实验测得平衡体系中气体组分转化率和氮气的体积分数的变化如图所示。
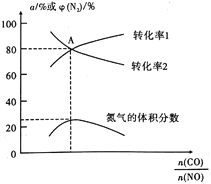
①根据图像推测转化率1曲线表示的是____________(填“CO”或“NO”)。
②A点时,![]() =_______________,氮气的体积分数为____________;T℃时,反应的平衡常数K=________________。
=_______________,氮气的体积分数为____________;T℃时,反应的平衡常数K=________________。
(4)已知:△G=△H-T△S;②△G=-RTlnK,其中K为反应的标准平衡常数,气体常数R=8.314×10-3kJ·mol-1·K-1。298K、101kPa时,2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)的△G=-687.6kJ·mol-1,该反应的△G>△H,原因是_________________。298K时,该反应的标准平衡常数K=___________(用含e的指数表示,列出计算式即可)。
2CO2(g)+N2(g)的△G=-687.6kJ·mol-1,该反应的△G>△H,原因是_________________。298K时,该反应的标准平衡常数K=___________(用含e的指数表示,列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2分子的结构如图所示: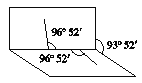 H2O2分子不是直线型的,两个H原子犹如在半展开的书的两面线上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:
H2O2分子不是直线型的,两个H原子犹如在半展开的书的两面线上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:
(1)写出H2O2分子的电子式________,其结构式为________。
(2)从极性键、非极性键角度写出分子内的化学键类型________。
(3)估计它难溶于CS2,简要说明原因______________________________________。
(4)指出氧元素的化合价,简要说明原因________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池用溴化锌溶液作电解液,并在电池间不断循环。下列有关说法正确的是
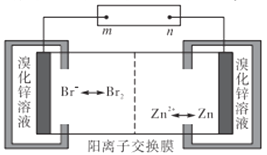
A. 充电时n接电源的负极,Zn2+通过阳离子交换膜由左侧流向右侧
B. 放电时每转移1mol电子负极区溶液质量减少65g
C. 充电时阴极的电极反应式为Br2+2e-=2Br-
D. 若将阳离子交换膜换成阴离子交换膜,放电时正负极也随之改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com