
某K2CO3与KHCO3的混合物共6.14 g,加热分解后质量减少为5.52 g。
(1)求原混合物中K2CO3的质量分数。(写出计算过程,计算结果精确到0.1%)
(2)若将原混合物溶于200 mL水配成溶液,向溶液中逐滴加入1.0 mol·L-1的稀盐酸。当加入的稀盐酸的体积为 mL时开始产生气体;当加入50 mL稀盐酸时,产生的气体在标准状况下的体积为 mL。
科目:高中化学 来源:2016届辽宁省分校高三上期中测试理综化学试卷(解析版) 题型:选择题
下列有关NaClO和NaCl混合溶液的叙述正确的是( )
A.该溶液中,H+、NH4+、SO42-、Br-可以大量共存
B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存
C.向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+ = Cl-+2Fe3++H2O
D.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上期中测试化学试卷(解析版) 题型:选择题
下列说法中有明显错误的是( )
A、对有气体参加的反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,反应速率增大
B、活化分子之间发生的碰撞一定为有效碰撞
C、升高温度,一般可使活化分子的百分数增大,因而反应速率增大
D、加入适宜的催化剂,可使活化分子的百分数大大增加,从而增大反应速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二上10月月考化学卷(解析版) 题型:填空题
固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。
(1)a点正反应速率___________(填大于、等于或小于)逆反应速率。
(2)下列时间段平均反应速率最大的是__________,最小的是______。
A.0~1min B.1~3min
C.3~8min D.8~11min
(3)求平衡时氢气的转化率和该条件下反应的平衡常数K。(写出计算过程)
(4)仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是___________,曲线II对应的实验条件改变是___________。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高一上12月月考化学卷(解析版) 题型:选择题
在酸性溶液中,下列物质氧化KI时,自身发生如下变化:IO3-→I2;MnO4-→Mn2+;Cl2→Cl?;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A.IO3- B.MnO4- C.Cl2 D.HNO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上二调考试化学试卷(解析版) 题型:选择题
相同条件下,现有四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。下列有关说法正确的是( )
A.由水电离出的c(H+):①=②=③=④
B.将②、③溶液混合后,pH=7,消耗溶液的体积:③=②
C.等体积的①、②、④溶液分别与足量铝粉反应,②生成的H2的物质的量最大
D.向溶液中加入100mL水后,溶液的pH:③>④>①>②
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中(文)化学试卷(解析版) 题型:选择题
全球气候变暖。据报道,江西在最近30年里平均气温升高142℃。下列哪些种气体的增加是导致这种情况出现的主要原因
A.N2 B.O2. C.CO2 D.SO2
查看答案和解析>>
科目:高中化学 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:填空题
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置 。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于______(填晶体类型).Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=______ .Fe(CO)x在一定条件下发生反应:
Fe(CO)x(s)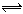 Fe(s)+ xCO(g)。已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型为 。
Fe(s)+ xCO(g)。已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型为 。
(3)写出CO的一种常见等电子体分子的结构式______;两者相比较沸点较高的为______(填化学式).CN-中碳原子杂化轨道类型为 ,S、N、O三元素的第一电离能最大的为 (用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图所示。

①基态铜原子的核外电子排布式为 。
②每个铜原子周围距离最近的铜原子数目 。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如附图所示(黑点代表铜原子)。
①该晶体的化学式为 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 (填“离子”、“共价”)化合物。
③已知该晶体的密度为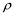 g.cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为 pm(只写计算式)。
g.cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为 pm(只写计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com