
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
| A、小于100mL |
| B、等于100mL |
| C、大于100mL |
| D、等于100/ρ mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
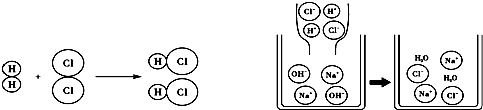
| A、该图可说明所有物质都是由分子构成的 |
| B、以上图示中未涉及置换反应 |
| C、两幅图表示的都是化合反应 |
| D、原子在化学变化中是可以再分的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
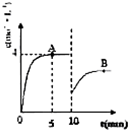 在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol?L-1和b mol?L-1,反应为:
在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol?L-1和b mol?L-1,反应为:查看答案和解析>>
科目:高中化学 来源: 题型:
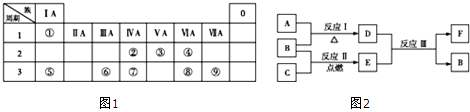
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol甲醇中含有C-H键的数目为4NA |
| B、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C、常温下,18g重水(D2O)所含的电子数为10NA |
| D、一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于氧化性HNO3大于H2SO4,所以非金属性:氮大于硫 |
| B、科学家在金属和非金属交界线处寻找催化剂 |
| C、只有主族元素是由短周期和长周期元素共同构成的 |
| D、长周期主族元素X的阳离子X2+的最外层有2个电子,则它是IVA族元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com