
| A. | 46g NO2和N2O4以任意比混合,所得混合气体中氧原子数2NA | |
| B. | 标准状况下,含NA个共价键的HF分子所占的体积约为22.4 L | |
| C. | 1mol Fe 与一定量的硝酸反应,转移的电子数为0.2NA~0.3NA | |
| D. | 2mol NO和1mol O2混合,在密闭容器中充分反应后,容器内的分子数小于2NA |
分析 A.NO2和N2O4分子中O的含量都是$\frac{32}{46}$,据此计算出混合物中含有的O的质量,然后根据n=$\frac{m}{M}$计算出其物质的量;
B.标准状况下,HF的状态不是气体;
C.铁与硝酸反应中,可以生成硝酸亚铁,也可以生成硝酸铁;
D.2mol NO和1mol O2混合恰好生成2mol二氧化氮,部分二氧化氮转化成四氧化二氮,所以反应后容器内分子的物质的量小于2mol.
解答 解:A.46g NO2和N2O4的混合物中含有氧元素的质量为:$\frac{32}{46}$×46g=32g,含有氧原子的物质的量为:$\frac{32g}{16g/mol}$=2mol,混合气体中氧原子数2NA,故A正确;
B.含NA个共价键的HF分子的物质的量为1mol,但是标准状况下HF不是气体,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.1mol Fe与一定量的硝酸反应,若完全生成硝酸亚铁,则失去2mol电子,若生成的是硝酸铁,失去3mol电子,所以转移的电子数为0.2NA~0.3NA,故C正确;
D.2molNO和1mol O2混合恰好生成2mol二氧化氮,由于二氧化氮与四氧化二氮之间存在转化平衡,则反应后容器内的分子的物质的量小于2mol,分子数小于2NA,故D正确;
故选B.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,明确标准状况下气体摩尔体积的使用条件为解答关键,注意熟练掌握物质的量与摩尔质量、阿伏伽德罗常数等之间的关系,试题培养了学生的分析能力及化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 地沟油经过处理,可用来制造肥皂 | |
| C. | 煤炭燃烧过程安装固硫装置,可有效提高煤的利用率 | |
| D. | 发生地震后,防疫人员在震区周围撒石灰,进行环境消毒,防止灾后出现疫情 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe3+ | B. | HS- | C. | 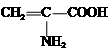 | D. | C6H5O- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,50g 98%浓硫酸和50g 98%浓磷酸混合后含氧原子数为4NA | |
| B. | 标准状况下,活泼金属与稀硫酸反应转移2NA个电子时,可产生22.4L气体 | |
| C. | 6.4g SO2溶于水配成1L溶液,含有H2SO3的分子数为0.1NA | |
| D. | 1mol C3H6分子中碳碳共价键数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO3溶液显酸性是因为:HSO3-+H2O?SO32-+H3O+ | |
| B. | 尼泊金酸(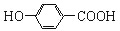 )与碳酸氢钠溶液反应: )与碳酸氢钠溶液反应: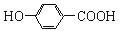 +2HCO3-→ +2HCO3-→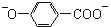 +CO2↑+2H2O +CO2↑+2H2O | |
| C. | KAl(SO4)2溶液中加入少量氢氧化钠溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 足量硫酸氢钠溶液与氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 其中含有的化学键的类型离子键、共价键
其中含有的化学键的类型离子键、共价键查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷 | |
| D. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com