
CH4(g)+H2O(g)![]() CO(g)+3H2(g);ΔH=+206.2 kJ·mol-1
CO(g)+3H2(g);ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g);ΔH=+247.4 kJ·mol-1
2CO(g)+2H2(g);ΔH=+247.4 kJ·mol-1
则
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:________. 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源:2011-2012学年海南省海南中学高二上学期期末考试理科化学试卷(带解析) 题型:填空题
(11分)(1)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为______________________________;
(2)在体积不变的密闭容器中进行(1)反应,达到平衡后(填“正向移动”、“逆向移动”、“增大”、“减小”或“不变”):
①扩大容器体积,平衡___________,c(H2)____________(与原平衡相比);
②升高温度,正反应速率________ ,逆反应速率___________;
体系的压强__________,平衡___________,平衡常数_____________;
③加入催化剂,H2的物质的量___________________。
查看答案和解析>>
科目:高中化学 来源:2013届浙江省杭州市建人高复学校高三第二次月考化学试卷(带解析) 题型:计算题
(10分)(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为 (阿伏伽德罗常数用NA表示),放出的热量为 kJ。
(2)已知:C3H8(g ) ==== CH4(g)+HC≡CH(g)+H2(g) △H1=156.6kJ·mol-1
CH3CH=CH2(g) ==== CH4(g)+HC≡CH(g) △H2=32.4kJ·mol-1
则相同条件下,反应C3H8(g)====CH3CH=CH2 (g)+H2(g)的△H= kJ·mol-1。
(3)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部分物质的燃烧热数据如右表:已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式 。
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省高三下学期一调考试理综化学试卷(解析版) 题型:填空题
二甲醚(CH3OCH3)是一种重要的精细化工产品,被认为是二十一世纪最有潜力的燃料[ 已知:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(1)? △H=-1455kJ/mol ]。同时它也可以作为制冷剂而替代氟氯代烃。工业上制备二甲醚的主要方法经历了三个阶段:
①甲醇液体在浓硫酸作用下或甲醇气体在催化作用下直接脱水制二甲醚; 2CH3OH  CH3OCH3+H2O
CH3OCH3+H2O
②合成气CO与H2直接合成二甲醚: 3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)?? △H=-247kJ/mol
CH3OCH3(g)+CO2(g)?? △H=-247kJ/mol
③天然气与水蒸气反应制备二甲醚。以CH4和H2O为原料制备二甲醚和甲醇工业流程如下:

(1)写出CO(g)、H2(g)、O2(g)反应生成CO2(g)和H2O(1)的热化学方程式(结果保留一位小数)????????????????????????????????????????????????
(2)在反应室2中,一定条件下发生反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是?????
CH3OCH3(g)+CO2(g)在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是?????
A.低温高压?? B.加催化剂??? C.增加CO浓度?? D.分离出二甲醚
(3)在反应室3中,在一定温度和压强条件下发生了反应:3H2(g)+CO2(g)  CH3OH(g)+H2O (g)? △H<0反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是??? (填序号)
CH3OH(g)+H2O (g)? △H<0反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是??? (填序号)

A.P3>P2?? T3>T2?????? B.P2>P4?? T4>T2
C.P1>P3 ? T1>T3?????? D.P1>P4?? T2>T3
(4)反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)? △H>0写出平衡常数的表达式:??????????????????????????
CO(g)+3H2(g)? △H>0写出平衡常数的表达式:??????????????????????????
如果温度降低,该反应的平衡常数????????????? (填“不变”、“变大”、“变小”)

(5)如图为绿色电源“二甲醚燃料电池”的工作原理示意图则a电极的反应式为:________________

(6)下列判断中正确的是_______
A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成
B.烧杯b中发生反应为2Zn-4eˉ =2Zn2+
C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极
D.烧杯a中发生反应O2 + 4H+ + 4eˉ = 2H2O,溶液pH降低
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省湛江市毕业班调研测试理综化学试卷(解析版) 题型:计算题
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4(g)+H2O(g) CO(g)+3H2(g)
△H=+206.0kJ•molˉ1
CO(g)+3H2(g)
△H=+206.0kJ•molˉ1
II:CO(g)+2H2(g) CH3OH(g)
△H=-129.0kJ•molˉ1
CH3OH(g)
△H=-129.0kJ•molˉ1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 。
(2)将1.0mol CH4和1.0mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应I,测得在一定的压强下CH4的转化率与温度的关系如图。
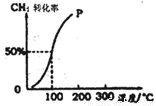
①假设100℃时达到平衡所需构时间为5min,则用H2表示该反应的平均反应速率为 。
②1000C时反应I的平衡常数为 。
(3)在压强为0.1 MPa、温度为300℃条件下,将a molCO与2a mol H2的混合气体在催化剂作用下发生反应II生成甲醇,平衡后将容器舶容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
A.平衡常数K增大 B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加 D.重新平衡c(H2)/c(CH3OH)减小
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将CO2+氧化成CO3+,然后以CO3+做氧化剂再把水中的甲醇氧化成CO2而净化。若下图装置中的电源为甲醇-空气-KOH溶液的燃料电池,则电池正极的电极反应式: ,该电池工作时,溶液中的OHˉ向 极移动。净化含1mol甲醇的水,燃料电池转移电子 mol。

查看答案和解析>>
科目:高中化学 来源:2010年广东省高三10月月考化学试题 题型:填空题
(12分)合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响。合成氨反应的化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。
2NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。
回答下列问题:
(1)合成氨工业中原料气压缩到30~50MPa的原因是 。从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是 。
(2)500℃、50MPa时,在容积为VL的容器中加入n mol N2、3n mol H2,反应达平衡后测得平衡常数为K,此时N2的转化率为x。则K和x的关系满足K= 。
(3)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部
分物质的燃烧热数据如下表:
|
物 质 |
燃烧热(kJ·mol-1) |
|
H2(g) |
-285.8 |
|
CO(g) |
-283.0 |
|
CH4(g) |
-890.3 |
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O(g)在高温下反应的热化学方程式 。
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。请写出该电池的正极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com