
【化学选修2化学与技术】(15分)氨气是工农业生产中重要的产品,合成氨并综合利用的某些过程如下图所示:

(1)原料气中的氢气来源于水和碳氢化合物。请写出甲烷和水在催化剂和高温条件下反应的方程式: 。
(2)在工业生产中,设备A的名称为 ,A中发生的化学反应方程式是 。
(3)上述生产中向母液通入氨气同时加入 ,可促进副产品氯化铵的析出。长期使用氯化铵会造成土壤酸化,尿素适用于各种土壤,在土壤中尿素发生水解,其水解的化学方程式是 。
(4)纯碱在生产生活中有广泛的应用,请写出任意两种用途: 。
(5)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。

①检验沉淀是否洗涤干净的方法是_________________________________。
②样品中NaCl的质量分数的数学表达式为__________________________。
(1)CH 4+2H2O=CO2+4H2 或 CH 4+H2O=CO+3H2(2分)
(2)沉淀池(1分);NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓(2分)。
(3)NaCl(1分);CO(NH2) 2+H2O=2NH3↑+CO2↑(2分)
(4)制玻璃、制皂、造纸、纺织、印染等(2分,其它合理答案也给分)
(5)①往少量的最后一次洗涤所得滤液中加入稀H2SO4溶液(或AgNO3溶液),若产生白色沉淀,则沉淀没有洗涤干净;若无白色沉淀,则沉淀已洗涤干净。(2分)
② (3分)
(3分)
【解析】
试题分析:(1)甲烷和水在催化剂和高温条件下反应的方程式为:CH 4+2H2O=CO2+4H2 或 CH 4+H2O=CO+3H2。(2)在工业生产中,设备A的名称为沉淀池,A中氨气、二氧化碳、氯化钠和水反应生成氯化铵和碳酸氢钠,化学反应方程式是NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓。(3)上述生产中向母液通入氨气同时加入NaCl,可促进副产品氯化铵的析出。尿素水解的化学方程式是CO(NH2) 2+H2O=2NH3↑+CO2↑。(4)纯碱在生产生活中的用途:制玻璃、制皂、造纸、纺织、印染等。(5)分析题给流程知测定纯碱样品中NaCl的质量分数的原理为向样品溶液中加入过量氯化钡溶液,碳酸钠转化为碳酸钡沉淀,通过测定碳酸钡的质量确定碳酸钠的质量,进一步确定氯化钠的质量,确定样品中NaCl的质量分数。①碳酸钡沉淀中含有过量的钡离子和氯离子,检验沉淀是否洗涤干净的方法是往少量的最后一次洗涤所得滤液中加入稀H2SO4溶液(或AgNO3溶液),若产生白色沉淀,则沉淀没有洗涤干净;若无白色沉淀,则沉淀已洗涤干净。②根据流程知碳酸钡的质量为ng,物质的量为n/197mol,根据碳酸根守恒知碳酸钠的物质的量为n/197mol,质量为106 n/197g,样品中NaCl的质量分数的数学表达式为 。
。
考点:考查化学与技术,涉及尿素的生产、氢气的工业制备及相关化学方程式的书写和计算。
考点分析: 考点1:化学与技术 试题属性

科目:高中化学 来源:2014-2015学年广东省、广雅中学、佛山一中高三联考理综化学试卷(解析版) 题型:实验题
(16分)硅孔雀石是一种含铜的矿石,含铜形态为CuCO3Cu(OH)2和CuSiO32H2O,同时含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。以硅孔雀石为原料制取硫酸铜的工艺流程如下:

(1)步骤①中稀硫酸与CuSiO3·2H2O发生反应的化学方程式: ;
用离子方程式表示双氧水的作用_______________________________________。
(2)步骤②调节溶液pH选用试剂不可以是__________________
a.CuO b.Cu (OH)2 c.Cu2(OH)2CO3 d.CuSO4
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
由上表可知当溶液pH=4时,可以完全除去的离子是______(填金属离子符号,后同),不能完全除去的离子是________。
(4)滤液B通过蒸发浓缩(设体积浓缩为原来的一半)、冷却结晶、洗涤可以得到CuSO45H2O晶体。某同学认为上述操作会有硫酸铝晶体析出。请你结合相关数据,通过计算对该同学的观点予以评价 (填“正确”、“不正确”、或“无法判断”)
【已知常温下,Al2(SO4)3饱和溶液中c(Al3+)=2.25mol/L,Ksp[Al(OH)3]=3.2×10-34】
(5)测定硫酸铜晶体(CuSO45H2O)里结晶水的含量,实验步骤为:a.研磨;b.称量空坩埚和装有试样的坩埚的质量;c.灼烧;d.干燥器中冷却;e.称量;f.重复c至e的操作,直到连续两次称量的质量差不超过0.1g为止;⑦根据实验数据计算硫酸铜结晶水的含量。
①步骤c用到的仪器有酒精灯、三脚架、泥三角、玻璃棒、 、 。
②步骤f的目的是 。
③如灼烧后在空气中冷却再称量,结晶水的测定结果会____(填“偏高”、“低”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2015年期中备考总动员高三化学模拟卷【福建】3(解析版) 题型:选择题
【改编】列与有机物的结构.性质有关的叙述正确的是
A.乙烯通入酸性KMn04溶液中,紫色褪去,是因为发生了加成反应
B.糖类、油脂、蛋白质都属于天然高分子化合物
C.葡萄糖.果糖的分子式均为C6H12O6,二者互为同分异构体
D.可用热的NaOH溶液除去乙酸乙酯中的乙酸杂质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省盟校高三第一次十校联考理综化学试卷(解析版) 题型:实验题
(15分)硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。它易溶于水,难溶于乙醇,加热、遇酸均易分解。工业上常用亚硫酸钠法、硫化碱法等制备。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:

实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3·5H2O。
④再经过滤、洗涤、干燥,得到所需的产品。
(1)写出仪器A的名称 步骤④中洗涤时,为了减少产物的损失用的试剂可以是 。
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因 。
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式 。
(4)最后得到的产品中可能含有Na2SO4杂质。请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: 。
(5)测定产品纯度
准确称取1.00 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。反应原理为2S2O32-+I2===S4O +2I-。滴定起始和终点的液面位置如图:则消耗碘的标准溶液体积为_______mL。产品的纯度为 %。
+2I-。滴定起始和终点的液面位置如图:则消耗碘的标准溶液体积为_______mL。产品的纯度为 %。

(6)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省盟校高三第一次十校联考理综化学试卷(解析版) 题型:选择题
有A、B、C、D四种短周期元素在周期表中位置如图所示。
…… | C | |||
A | B | …… | D |
已知:A2+与C原子的电子数相差2。下列推断不正确的是
A.A和D组成的化合物是弱电解质且水溶液呈酸性
B.与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应中常作催化剂。
C.离子半径:C>A>B
D.B与C形成的化合物是冶金工业的一种原料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省红色六校高三第二次联考理综化学试卷(解析版) 题型:选择题
电化学降解NO3-的原理如图所示。下列说法中正确的是

A.铅蓄电池的A极为负极,电极材料为Pb
B.铅蓄电池工作过程中每通过电路中2mol电子则消耗1molH2SO4
C.该电解池的阴极反应为2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移5moL电子,则交换膜两侧电解液的质量变化差(Δm左—Δm右)为14.4g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高三第三次四校联考理综化学试卷(解析版) 题型:填空题
选考[化学---选修3:物质结构与性质] (15分)
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)铟与镓同是IIIA族元素,写出铟基态原子的电子排布式: 。
(2)硒为第四周期VIA族元素,与其相邻的元素有砷(33号)、溴(35号),则三种元素的电负性由小到大的顺序为 。(用元素符号表示)
(3)SeO3分子的立体构型为 。
(4)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是 。

(5)硼元素具有缺电子性,其化合物往往具有加合性,如硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-,其中B原子的杂化类型为 。
(6)金属铜投入氨水中或投入H2O2溶液中均无明显现象,但投入氨水—过氧化氢混合液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子方程式: 。
(7)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数比为 ;若该晶体的晶胞参数为a pm,则该合金密度为 g/cm3。(列出计算式,不要求计算结果,阿伏伽德罗数的值为NA)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省宿迁市三校高三下学期3月质量检测化学试卷(解析版) 题型:推断题
(15分)葛根大豆苷元(F)用于治疗高血压引起的头疼、突发性耳聋等症,其合成路线如下:

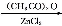
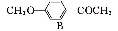








(1)化合物C中的含氧官能团有 、 (填官能团名称)。
(2)已知:C D为取代反应,其另一产物为H2O,写出X的结构简式: 。
D为取代反应,其另一产物为H2O,写出X的结构简式: 。
(3)反应E F的反应类型是 。
F的反应类型是 。
(4)写出同时满足下列条件的B的两种同分异构体的结构简式: 。
Ⅰ.属于芳香族化合物,分子中有4种不同化学环境的氢
Ⅱ.能与FeCl3溶液发生显色反应
Ⅲ.不能发生水解反应,能发生银镜反应
(5)根据已有知识并结合相关信息,写出以 和(CH3CO)2O为原料制备药物中间体
和(CH3CO)2O为原料制备药物中间体 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C CH2
CH2 CH3CH2Br
CH3CH2Br CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2014-2015河北枣强中学高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是: 。
不采用铜跟浓硫酸反应来制取硫酸铜的原是 。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180 mL。
(3)若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 。
(4)将8 g Fe2O3投入到150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,收集到1.68 L H2(标准状况),同时,Fe和Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的物质的量浓度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com