
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+��H2 |
| B��MnO4-��Mn2+ |
| C��CO2��CO32- |
| D��S2-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
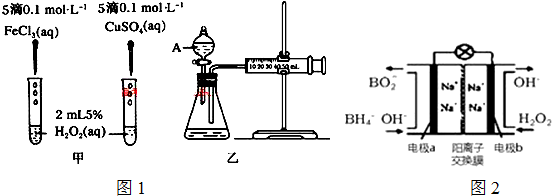
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
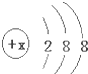 �м���Ԫ�ص�����������Ӳ�ṹ��ͼ��ʾ�����У�
�м���Ԫ�ص�����������Ӳ�ṹ��ͼ��ʾ�����У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ���ϵ����� | ���ʵĻ�ѧʽ������ |
| ��1�� | ����� | |
| ��2�� | ����ʣ�������״̬�²������� | |
| ��3�� | ����ʣ���������ˮ | |
| ��4�� | ����������ǵ���� | |
| ��5�� | ���ǵ���ʣ��������ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼�������Һ�м��������NaOH��Һ��Ca2++HCO3-+OH-=CaCO3��+H2O |
| B��NaHSO4��Һ��Ba��OH��2��Һ��Ϻ������ԣ�Ba2++OH-+H++SO42-=BaSO4��+H2O |
| C��FeI2��Һ��ͨ������Cl2��2 Fe2++Cl2=2 Fe3++2Cl- |
| D����NH4Al��SO4��2��Һ�е���Ba��OH��2��ҺǡʹSO42-������ȫNH4++Al3++2Ba2++2SO42-+4OH-=Al��OH��3��+NH3?H2O+2BaSO4�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com