
����Ŀ����ѧʵ�����һ�����Ż������п��Ũ����ķ�Ӧ��С����Ϊ�����������Ƕ�������ָ����ʦ����ʦָ�������������������⣬�����ܲ���������Ϊ����֤�����ж��Ƿ���ȷ��ͬѧ��չ���˼��ҵ����ۣ�������Ȥ�������ͼ��ʾʵ��װ�ã�п��Ũ���Ṳ��ʱ����������ΪX���Ҹ�װ����ȥ�����Իش��������⣺ 
��1�����ɶ�������Ļ�ѧ����ʽΪ��
��2������ʦ��Ϊ�����ܲ��������������ǣ�
��3��ͬѧ���ڰ�װ��װ�úز����ٵ�һ�������ǣ�
��4��A�м�����Լ������� �� ��������B�м�����Լ������� �� ��������E�м�����Լ������� �� ������ ��
��5������֤������X�к���������ʵ�������ǣ�C�У� �� D�У� �� ���ȥ��װ��B�����ܷ����D�е������ж�����X��������������ܡ����ܡ�����ԭ���� ��
���𰸡�
��1��Zn+2H2SO4��Ũ�� ![]() ZnSO4+SO2��+2H2O
ZnSO4+SO2��+2H2O
��2����Zn��ŨH2SO4��Ӧʱ,ŨH2SO4Ũ����ϡ,Zn��ϡH2SO4��Ӧ�ɲ���H2
��3�����װ�õ�������
��4��Ʒ����Һ������SO2��ŨH2SO4������ˮ��������ʯ�ң���ֹ�����е�ˮ��������D��
��5����ɫ�����ɺ�ɫ����ɫ��ĩ�����ɫ�����ܣ���Ϊ��������к�H2O,�����H2�ļ���
���������⣺��1��п��Ũ���ᷴӦ�Ƕ�����������п��ˮ����Ӧ�Ļ�ѧ����ʽΪZn+2H2SO4��Ũ�� ![]() ZnSO4+SO2��+2H2O��
ZnSO4+SO2��+2H2O��
���Դ��ǣ�Zn+2H2SO4��Ũ�� ![]() ZnSO4+SO2��+2H2O����2����ӦʱŨH2SO4 Ũ����ϡ��Zn��ϡH2SO4 ��Ӧ�ɲ���H2����Ӧ�Ļ�ѧ����ʽΪ��Zn+H2SO4=ZnSO4+H2����
ZnSO4+SO2��+2H2O����2����ӦʱŨH2SO4 Ũ����ϡ��Zn��ϡH2SO4 ��Ӧ�ɲ���H2����Ӧ�Ļ�ѧ����ʽΪ��Zn+H2SO4=ZnSO4+H2����
���Դ��ǣ���Zn��ŨH2SO4��Ӧʱ��ŨH2SO4Ũ����ϡ��Zn��ϡH2SO4��Ӧ�ɲ���H2����3��װ����������֤ʳ�Σ�������Ҫװ����������ã�ʵ�鿪ʼ�ȼ���װ�õ������ԣ�
���Դ��ǣ����װ�õ������ԣ���4������װ��ͼ��֪�����ɵ��������ж������������������װ��A����֤����������ڵ�װ�ã�ѡƷ����Һ������֤��ͨ�����������Һ��ȥ��������ͨ��װ��B�е�Ũ�����ȥˮ��������������������ͭ��Ӧ����ͭ��ˮ��������������װ��D�� ����ˮ����ͭ����ˮ�����ɣ�Ϊ��������е�ˮ����Ӱ��Dװ����ˮ�ļ��飬װ��E����Ҫ�ü�ʯ�ң�
���Դ��ǣ�Ʒ����Һ������SO2�� ŨH2SO4������ˮ��������ʯ�ң���ֹ�����е�ˮ��������D�У���5��֤�����ɵ������к���ˮ����������Cװ���к�ɫ����ͭ��Ϊ��ɫͭ��Dװ���а�ɫ����ͭ��Ϊ��ɫ�����ȥ��װ��B����������к�H2O�������H2�ļ��飬����ȥ��Bװ�ã�
���Դ��ǣ���ɫ�����ɺ�ɫ����ɫ��ĩ�����ɫ�����ܣ���Ϊ��������к�H2O�������H2�ļ��飮


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ת����ϵ�У�X��Y����������������;�㷺�����ֽ������ʣ�A��B�������A�ʺ���ɫ��C��D��E����ѧ���������ֻ��������ת����ϵ�ش����⣺ 
��1����д����Ӧ�ٵĻ�ѧ����ʽ ��
��2���Լ�a����Һ��дһ�ּ��ɣ�
��3�����Լ�b��H2SO4 �� ��ҵ����E��H2SO4��NaNO2 Ϊԭ����ȡ��Ч��ˮ��Y��OH��SO4 �� ��֪��ԭ����ΪNO����÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������⣮ I����֪����Ϊ��ѧ�����������ʣ����Ͷ�Ϊ�������嵥�ʣ�A��EΪ���������AΪ����ɫ���壬������BΪҺ�壬C����ɫ��ӦΪ��ɫ���Իش��������⣺
��1��A�� E�Ļ�ѧʽ�ֱ�Ϊ����
��2��A+B��C+���Ļ�ѧ����ʽ����
��3��D+C��B+E�����ӷ���ʽ����
��4��1mol��1mol�һ��Ͷ��������B�У��ڱ�״��������ܲ���L�����壮
��5��II���ڱ�״���£�ȡ�ס��ҡ�����30��mL��ͬŨ�ȵ����ᣬȻ��ֱ��������������ͬ��þ���������±����й����ݣ���Ӧǰ����Һ����������仯����
ʵ����� | �� | �� | �� |
���������/mg | 255 | 385 | 459 |
�������/mL | 280 | 336 | 336 |
�ټ���ʵ���У�������������������������㡱��������ʵ���У�������������������������㡱��
����������ʵ���Ũ��Ϊmol/L����
�ۻ������Mg��Al�����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��װ�õ�˵������ȷ���ǣ� ��
A.
��ͼװ����ȡ���﴿����NH3
B.
��ͼװ��ʵ�����Ʊ�Fe��OH��2
C.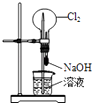
��ͼװ�ÿ�����ɡ���Ȫ��ʵ��
D.
��ͼװ�ò���Cu��Ũ���ᷴӦ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH������9��NaOH��CH3COONa������Һ�У�����ˮ���������OH������Ũ�ȷֱ�Ϊamol/L��bmol/L����a��b��ϵΪ�� ��
A.a��b
B.a=10��4 b
C.b=10��4 a
D.a=b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijǿ������ҺX�����ܺ���Al3+��Ba2+��NH4+��Fe2+��Fe3+��CO32����SO42����SiO32����NO3���е�һ�ֻ������ӣ�ȡ����Һ����ʵ�飬������ת����ͼ����һ�������Ǻ���ɫ����ش��������⣺ 
��1����ҺX�г���H+һ�����ڵ������� �� ��ҺX��һ�������ڵ������� ��
��2����������A�����ӷ���ʽΪ ��
��3��ת��������Ӧ������Ϊ ��
��4��ת�� ���е����ӷ���ʽΪ ��
��5����ת�����У�D��H2O��O2��������ǡ�÷������Ϸ�Ӧ����E����Ӧ��O2��D�����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йػ�ѧ��Ӧ��˵���У���ȷ���ǣ� ��
A.���Է���Ӧ���κ������¶�����ʵ��
B.�Է���Ӧ����������ķ�Ӧ
C.���Է����е����ȷ�Ӧһ����������ķ�Ӧ
D.�Է���Ӧ���Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڵؿ�����Ҫ��NaIO3 �� ����ʽ���ڣ��ں�ˮ����Ҫ��I������ʽ���ڣ���������֮���ת����ϵ��ͼ��ʾ������˵���в���ȷ���ǣ� �� 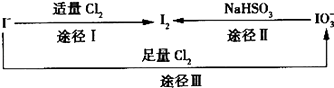
A.�õ��۩�KI��ֽ��ʳ����ӵ���ʱ���۩�KI��ֽ�����
B.����Cl2��ʹʪ��ġ��ѱ����ĵ��۩�KI��ֽ��ɫ��ԭ�������5Cl2+I+6H2O�T2HI03+10HCl
C.��ͼ��֪�����Ե�ǿ��˳��ΪCl��I��IO ![]()
D.;������������1 mol I����Ӧ��ת�Ƶĵ�����Ϊ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ӷ�Ӧ���漰H2O��ClO����NH4+��H+��N2��Cl��������������N2��ClO�������ʵ�����ʱ��仯����������ͼ��ʾ�������жϲ���ȷ���ǣ� �� 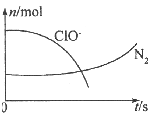
A.�÷�Ӧ����������ClO��
B.����1 mol��ԭ����ת��3 mol����
C.�������뻹ԭ�������ʵ���֮��Ϊ2��3
D.��Ӧ����Һ������������ǿ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com