
����Ŀ��F ����Ҫ���л�����������ɻ��������� A ͨ�����¹����Ƶã�
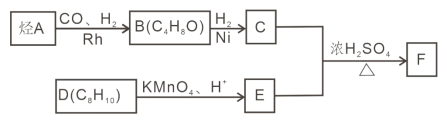
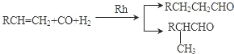
��֪����
���˴Ź���������ʾ C �ķ����к��� 4 �ֲ�ͬ��ѧ��������ԭ�ӣ���������֮��Ϊ6:1:2:1��
��F�������������б����ϵ�һ��ȡ����ֻ�����֡�
��1��A �����Ӿ۷�Ӧ�Ļ�ѧ����ʽ��_____��
��2��B �� �� �� �� �� Ϊ _____�� �� �� B �� �� �� �� �� ʵ �� �� �� ����___________��
��3��F �еĹ����ŵ�����Ϊ_____��C+E��F �Ļ�ѧ����ʽ��_____��
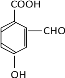
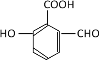
��4��X �� E ��Ϊͬ���칹�壬�� X �����������ʣ����������� X ��_____�֣������������칹����
�ٷ����к��б����������� NaHCO3 ��Һ��Ӧ���ɶ�����̼����
����������Һ�������������ɡ�
��5���������ϩ�ͱ�Ҫ����ԭ�Ϻϳɱ��������ĺϳ�·��_______________��
���𰸡�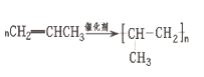 2-����ȩȡ���� B ���Թ��У�����������Һ��ˮԡ����һ��ʱ�䣬���������������ɣ� ��֤����ȩ�������������������ͭ����Һ�����ȣ����۲쵽��ש��ɫ�������ɣ���֤����ȩ��������
2-����ȩȡ���� B ���Թ��У�����������Һ��ˮԡ����һ��ʱ�䣬���������������ɣ� ��֤����ȩ�������������������ͭ����Һ�����ȣ����۲쵽��ש��ɫ�������ɣ���֤����ȩ��������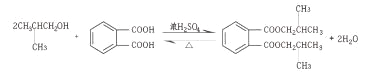 13 ��
13 ��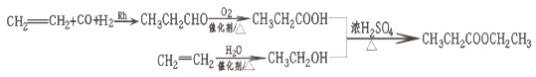
��������
��A������Ϣ���еķ�Ӧ����B�����B�ķ���ʽ��֪AΪCH2=CHCH3��BΪȩ��B��H2�����ӳɷ�Ӧ����CΪ����C�ķ����к���4�ֲ�ͬ��ѧ��������ԭ�ӣ���������֮��Ϊ6:1:2:1����CΪ![]() ����BΪ
����BΪ![]() ��C��E��Ӧ����F��F���������ҷ����к��б�������֪E�����Ȼ���������F�����б����ϵ�һ��ȡ����ֻ�����֣����D����ʽ��֪DΪ
��C��E��Ӧ����F��F���������ҷ����к��б�������֪E�����Ȼ���������F�����б����ϵ�һ��ȡ����ֻ�����֣����D����ʽ��֪DΪ![]() ����E
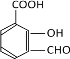
����E![]() ��FΪ
��FΪ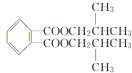 ��
��
(1).AΪCH2=CHCH3�������Ӿ۷�Ӧ���ɾ۱�ϩ����ѧ����ʽΪ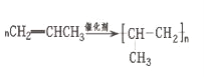 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
(2).BΪ![]() ��������2-����ȩ��B�еĹ�������ȩ��������ȩ����ʵ�鷽����ȡ���� B ���Թ��У�����������Һ��ˮԡ����һ��ʱ�䣬���������������ɣ� ��֤����ȩ�������������������ͭ����Һ�����ȣ����۲쵽��ש��ɫ�������ɣ���֤����ȩ�������ʴ�Ϊ��2-����ȩ��ȡ���� B ���Թ��У�����������Һ��ˮԡ����һ��ʱ�䣬���������������ɣ� ��֤����ȩ�������������������ͭ����Һ�����ȣ����۲쵽��ש��ɫ�������ɣ���֤����ȩ������
��������2-����ȩ��B�еĹ�������ȩ��������ȩ����ʵ�鷽����ȡ���� B ���Թ��У�����������Һ��ˮԡ����һ��ʱ�䣬���������������ɣ� ��֤����ȩ�������������������ͭ����Һ�����ȣ����۲쵽��ש��ɫ�������ɣ���֤����ȩ�������ʴ�Ϊ��2-����ȩ��ȡ���� B ���Թ��У�����������Һ��ˮԡ����һ��ʱ�䣬���������������ɣ� ��֤����ȩ�������������������ͭ����Һ�����ȣ����۲쵽��ש��ɫ�������ɣ���֤����ȩ������
(3).F�Ľṹ��ʽΪ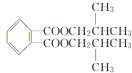 �������ŵ�������������CΪ
�������ŵ�������������CΪ![]() ��EΪ
��EΪ![]() �����߷���������Ӧ����F����ѧ����ʽΪ
�����߷���������Ӧ����F����ѧ����ʽΪ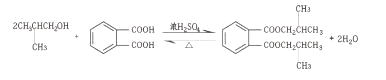 ���ʴ�Ϊ��������
���ʴ�Ϊ�������� ��
��
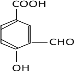
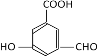
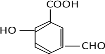
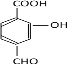
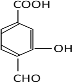
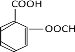
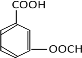
(4). EΪ![]() ��X �� E ��Ϊͬ���칹�壬�� X �����������ʣ��ٷ����к��б����������� NaHCO3 ��Һ��Ӧ���ɶ�����̼���壬˵�������к��С���COOH���� ����������Һ�������������ɣ�˵�������к��С���OOCH����OH���͡���CHO������ϣ������������У�
��X �� E ��Ϊͬ���칹�壬�� X �����������ʣ��ٷ����к��б����������� NaHCO3 ��Һ��Ӧ���ɶ�����̼���壬˵�������к��С���COOH���� ����������Һ�������������ɣ�˵�������к��С���OOCH����OH���͡���CHO������ϣ������������У�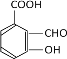 ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
��![]() ����13�����ʴ�Ϊ��13����
����13�����ʴ�Ϊ��13����
(5).��ϩ������Ϣ�ٷ�Ӧ���ɱ�ȩ����ȩ��������Ӧ���ɱ��ᣬ��ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ����Ҵ�����ᷢ��������Ӧ���ɱ����������ϳ�·��Ϊ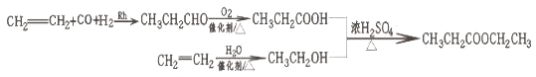 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�ѧ�������������ת����˵����ȷ���ǣ� ��

A. ͼ1��ʾ��װ���ܽ���ѧ��ת��Ϊ����
B. ͼ2��ʾ�ķ�ӦΪ���ȷ�Ӧ
C. �кͷ�Ӧ�У���Ӧ��������������������������
D. ��ѧ��Ӧ�������仯����Ҫԭ���ǻ�ѧ���Ķ������γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڼ��������¿ɻ�ԭ����ͭ����������ˮ�����⣬����̼�������ij��ѧС��������ͼװ��̽���䷴Ӧ���

[��������]��CO����������Һ��Ӧ��CO��2[Ag(NH3)2]����2OH��===2Ag����2NH4+��CO32����2NH3��
��Cu2OΪ��ɫ������Ag+��Ӧ���ܷ�����Ӧ��Cu2O��2H��===Cu2+��Cu��H2O��
��1��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��2�������������װ�ô����ҵ�����˳��ΪA��__________________��(����ĸ���)
��3��ʵ���еμ�ϡ����IJ���Ϊ______________________________________________��
��4����֪��������к���CO����װ��C�пɹ۲쵽��������________________��װ��F������Ϊ_________________________________________��
��5������Ӧ������װ��D���Թ��й���ȫ����Ϊ��ɫ��
�����ʵ��֤����ɫ�����к���Cu2O��______________________________________________��
����֤����ɫ�������Ƿ���Cu����ͬѧ�������ʵ�飺��������ɫ�����м�������0.1mol��L1AgNO3��Һ��������Һ�������ݴ��жϺ�ɫ�����к���Cu����ͬѧ��Ϊ�÷�������������֤����ͬѧ�Ľ��ۣ������������¶Ա�ʵ�飬��ɱ������ݡ�
ʵ�鲽��(��Ҫ��д�������������) | Ԥ������ͽ��� |
__________________ | ���۲쵽��Һ����������֤����ɫ�����к���Cu�����۲쵽��Һ����������֤����ɫ�����к���Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2017��2��19���ڵ�ʮ���찢�����ȹ��ʷ���չ�ϣ������Ƚ�����ȼ�ϵ��ϵͳ�����˻��������˸ü���270�����������������¼�������й���ȼ�ϵ�ص�˵������ȷ����
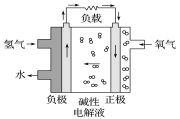
A. ͨ�������ĵ缫����������Ӧ
B. ���Ե��Һ����������ͨ�������ķ����ƶ�
C. �����ĵ缫��ӦʽΪO2��2H2O��4e��===4OH��
D. �ŵ�����м��Ե��Һ��OH�������ʵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɷе����ݣ����飭161.5�棬���飭88.6�棬�����飭0.5�档����ķе�����ǣ� ��
A.���ڣ�0.5��
B.Լ��30��
C.Լ�ǣ�40��
D.���ڣ�88.6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л������������ȷ����
A. �л���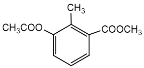 �ĺ˴Ź�������ͼ����4�����͵���ԭ�����շ�
�ĺ˴Ź�������ͼ����4�����͵���ԭ�����շ�
B. ��FeCl3��Һ���Լ��𱽡����ӡ����Ȼ�̼��KSCN���Ҵ���AgNO3������ɫ��Һ��Һ��
C. �л���Ӧ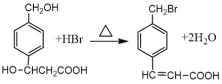 �漰ȡ����Ӧ����ȥ��Ӧ��������
�漰ȡ����Ӧ����ȥ��Ӧ��������
D. 1 mol 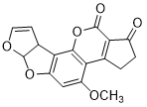 һ����������������6 mol H2��Ӧ
һ����������������6 mol H2��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ṹ��������ƽ�������νṹ��������(����)
A.CH3Cl������ͬ���칹��
B.CH2Cl2������ͬ���칹��
C.CHCl3������ͬ���칹��
D.�����ǷǼ��Է���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�����Ԫ�����ڱ���һ���֣��밴Ҫ�����
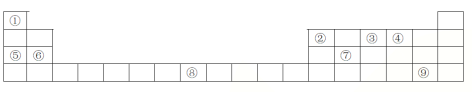
��1��Ԫ���������γɵĻ������д��ڵĻ�ѧ������Ϊ__________________
��2��д�����٢ڢ��γɵ�һ��һԪ��ķ���ʽ_________________
��3��д�������γɵĵ��ʵĵ���ʽ_________________
��4���о�Ԫ�����γɵ�������һ����;________________��Ԫ���������ڱ��е�λ�� ____��
��������ŷḻ�ĺ�ˮ��Դ����ˮ��Ԫ���ݡ��������ĺ����ܷḻ��ij��ѧ��ȤС���Ƚ���ˮ������õ�ˮ���ٴ�ʣ���Ũ��ˮ��ͨ��һϵ�й�����ȡ������Ʒ����ش���������
�ش��������⣺
��5����ˮ�����ķ�����Ҫ��___________________________________(�����о�2��)
��6����������������������Ũ��ˮ�д���Br2�������£�Br2����ɫΪ___________________��
���������ô�����Һ���գ����������Ҫ��Ӧ��Br2+Na2CO3+H2O��NaBr+NaBrO3+ NaHCO3(δ��ƽ)��������1mol Br2ʱ��ת�Ƶĵ�����Ϊ________mol��
��7���Ӻ�ˮ�л��Ԫ���������Ļ������һ�ι���������ͼ��
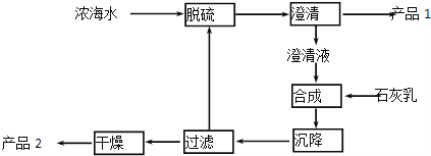
Ũ��ˮ����Ҫ�ɷ�����:
���� | Na+ | Mg2+ | Cl- | SO42- |
Ũ��/(g��L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
�ù��չ����У���Ʒ1�Ļ�ѧʽΪ________________����Ʒ2ΪMg(OH)2����������Ũ��ˮ�еμ�NaOH��Һ����Mg2+ǡ����ȫ����ʱ��Һ��pHΪ_________��(��֪25��ʱKsp[Mg(OH)2]=1.0��10-13)
��8������MgCl2��6H2O�����Ʊ�MgCl2ʱ��ʵ����ȡ�óɹ��Ĺؼ�������������_________��
����ʯī���������������������ڵ��Ȼ�þ��������Ӧ�Ļ�ѧ����ʽΪ______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����ڹ�ҵ��������������;�dz��㷺���ش��������⣺
��1����̬��ͭ���Ӽ۵����Ų�ʽΪ____________����һ������I(Cu)________I (Zn)�������������ԭ��__________________________________________��
��2��Cu(CH3CN)42+���İ���ͭ���ӻ��ȶ�����������Cu����λ����_______��������̼ԭ�ӵ��ӻ�������_________________,1molCH3CN�ЦҼ��ĸ���Ϊ_____________��
��3��CuCl���л��ϳ��г���������CuCl�ۻ��������磬�Ʋ�CuCl�����л�ѧ������Ϊ_________��CuCl��ǿ�Ȼ�ֽ�����ͭ��ͭ����Ķѻ���ʽΪ__________�������ֱ�ʾ����
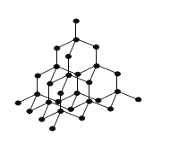
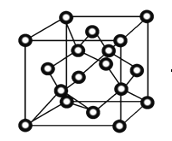
��4��������Ľṹ����ʯ�Ľṹ���ƣ���������ϵ����ͼ�������ʯ�����е�Cԭ��ȫ���û���Oԭ�ӣ�Oԭ�������������ĸ�Oԭ��������Hԭ�Ӳ�������������Oԭ��֮�䣬�����γ�һ�����ۼ���һ���������Ϊ���еĹ��ۼ��������0��ʱ������������ļ�����A��H��B��Ϊ_______________pm����ʽ�����㣩����0��ʱ���ܶ�Ϊ0.9g�Bcm-3��![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com