
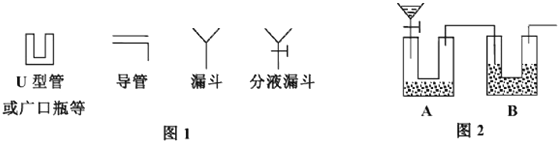

���� ����������������ʵ��װ�òⶨ̼���ƴ��ȵĹ����ǣ�Ũ�����������ˮ��ϡ�ͳ�ϡ���ᣬ����ϡ�����п����Aװ���з�����Ӧ��������������������װ��C�����ɵĶ�����̼ȫ������װ��E��ȫ�����գ�B������Ҫװ�ã�װ��C��CaCO3 �����ϡ���ᷴӦ���ɶ�����̼��װ��D����Ũ�������������еĶ�����̼������װ��E�������ɵĶ�����̼����ⶨ����������õ�̼���Ƶ��������㴿�ȣ�F װ���еļ�ʯ�ҵ������Ƿ�ֹ�����е�ˮ������������̼����װ��EӰ��ⶨ�����
��1��A�����ɵĶ�����̼���岻��ȫ������B�����գ�A�����������ˮ����Ҳ����B�ȣ�
��2��Ũ���������ˮ�ԣ��ڽ����ʯ��ǰ��������Ũ�����ȥ�����е�ˮ������
��3������װ��A��������A�����ɵ�����ʹC�����ɵĶ�����̼ȫ��������װ��E����ȫ���գ�Fװ���еļ�ʯ�ҿ������տ�����ˮ�����Ͷ�����̼���������װ��EӰ��ⶨ�����
��4���������ɵĶ�����̼�������㷴Ӧ��̼���ƣ�����=$\frac{������}{��Ʒ��}$��100%��
��5��H2A �ĵ�һ������H2A?H++HA-���ڶ�������ΪHA-?H++A2-��ƽ�ⳣ��Ka1=$\frac{c��{H}^{+}��c��H{A}^{-}��}{c��{H}_{2}A��}$��Ka2=$\frac{c��{H}^{+}��c��{A}^{2-}��}{c��H{A}^{-}��}$��HA-+H2O?H2A+OH-��Kh=$\frac{c��O{H}^{-}��c��{H}_{2}A��}{c��H{A}^{-}��}$=$\frac{c��O{H}^{-}��c��{H}_{2}A��}{c��H{A}^{-}��}$��$\frac{c��{H}^{+}��}{c��{H}^{+}��}$=$\frac{Kw}{{K}_{a1}}$��
��� �⣺��1��ʵ����ֽϴ�ƫ���ԭ����U�ι�A�е�CO2����δȫ������U�ι�B��U�ι�A�еķ�Ӧ��������ˮ��������U�ι�B��ʹ�ü�ʯ�����ص�������ȫ��CO2������
�ʴ�Ϊ��U�ι�A�е�CO2����δȫ������U�ι�B��U�ι�A�еķ�Ӧ��������ˮ��������U�ι�B��ʹ�ü�ʯ�����ص�������ȫ��CO2������
��2��B�в���װ�ã�D�м�һ��ʢŨH2SO4��ϴ��ƿ��װ��ͼΪ��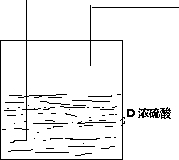
�ʴ�Ϊ�� ��
��
��3��Ũ�����������ˮ��ϡ�ͳ�ϡ���ᣬ����ϡ�����п����Aװ���з�����Ӧ��������������������װ��C�����ɵĶ�����̼ȫ������װ��E��ȫ�����գ�F װ���еļ�ʯ�ҵ������Ƿ�ֹ�����е�ˮ������������̼����װ��EӰ��ⶨ�����
�ʴ�Ϊ��A�����ɵ�H2ʹC�е�CO2����ȫ����E�еļ�ʯ�����գ����տ����н����ˮ������CO2�����壻
��4����10.0g Na2CO3��Ʒ��̼��������Ϊx��E װ���������� 3.96gΪ���ɵĶ�����̼������
Na2CO3+H2SO4=Na2SO4+CO2��+H2O
106 44
x 3.96g
x=9.54g��
Na2CO3�����Ĵ���=$\frac{9.54g}{10.0g}$��100%=95.4%��
�ʴ�Ϊ��95.4%��
��5���� 0.1mol•L-1�� H2A ��Һ�ڳ����µ� pH=3��c��A2-��=1��10-6mol•L��H2A �ĵ�һ������H2A?H++HA-���ڶ�������ΪHA-?H++A2-��ƽ�ⳣ��Ka1=$\frac{c��{H}^{+}��c��H{A}^{-}��}{c��{H}_{2}A��}$��Ka2=$\frac{c��{H}^{+}��c��{A}^{2-}��}{c��H{A}^{-}��}$=$\frac{1{0}^{-3}��1{0}^{-6}}{1{0}^{-3}}$=10-6��Ka1=$\frac{1{0}^{-3}��1{0}^{-3}}{0.1}$=10-5��
HA-+H2O?H2A+OH-��Kh=$\frac{c��O{H}^{-}��c��{H}_{2}A��}{c��H{A}^{-}��}$=$\frac{c��O{H}^{-}��c��{H}_{2}A��}{c��H{A}^{-}��}$��$\frac{c��{H}^{+}��}{c��{H}^{+}��}$=$\frac{Kw}{{K}_{a1}}$=$\frac{1{0}^{-14}}{1{0}^{-5}}$=10-9��
�ʴ�Ϊ��10-6��10-9��
���� ���⿼����hi��ɵ�ʵ��̽����ʵ��װ�ú��Լ������÷�������Ʒ���ȵ�ʵ��ⶨ������������ʵ���ƽ�ⳣ����������ˮ��ƽ�ⳣ���ļ����֪ʶ�㣬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ͻ���۵�һ�����ֽ����� | B�� | �Ͻ���ֻ������Ԫ�� | ||
| C�� | �Ͻ�Ļ�е����һ�����ֽ����� | D�� | �Ͻ��Ӳ��һ������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��CO2�������ƣ�������ˮ��Һ�б��������� | |
| B�� | Na2O2��Na2O���Ԫ����ͬ����CO2��Ӧ����Ҳ��ͬ | |
| C�� | Mg��K��һ����������ˮ��Ӧ������H2�Ͷ�Ӧ�ļ� | |
| D�� | Na��Liͬ���ڼ�������ʣ��ڼ�����������������Ӧ�����ɹ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������=A-n | B�� | ������=Z+A | C�� | ����������=Z+n | D�� | ����������=A-Z |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | I�͢� | B�� | I��IV | C�� | ��͢� | D�� | ���IV |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������2 | B�� | ��������2 | C�� | ��������3 | D�� | ��������1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com