
| A、标准状况下,22.4LCO和CO2混合气体中含有的碳原子数约为NA |
| B、1mol苯分子中含有的碳碳双键数为3NA |
| C、常温常压下,0.1mol铁在Cl2中充分燃烧,转移的电子数为0.3 NA |
| D、1L1mol/L的Na2CO3溶液中离子总数大于3NA |


科目:高中化学 来源: 题型:
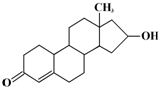 “诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图.下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图.下列关于“诺龙”的说法中不正确的是( )| A、分子式是C18H26O2 |
| B、具有酚的化学性质 |
| C、具有烯的化学性质 |
| D、具有酮的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极发生的反应为:Fe-2e-=Fe2+ |
| B、正极发生的反应为:4OH--4e-═2H2O+O2↑ |
| C、原电池是将电能转变为化学能的装置 |
| D、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| B、1 mol Cl2与足量的铁反应,转移的电子数为3NA |
| C、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10 NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、氯化铝溶液中加入足量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| C、氯化铁溶液中加入铁粉:Fe3++Fe═2Fe2+ |
| D、氯化亚铁溶液跟氯气反应:Fe2++Cl2═Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴化亚铁溶液中通入过量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
| B、草酸和少量烧碱溶液:H2C2O4+2OH-═C2O42-+2H2O |
| C、漂白粉溶液吸收过量的二氧化碳:ClO-+H2O+CO2═HClO+HCO3- |
| D、将铜片投入足量稀硝酸:Cu+NO3-+4H+═Cu2++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CO | H2O(g) | CO2 | H2 |
| 初始浓度/mol?L-1 | 1 | 1 | 0 | 0 |
| 平衡浓度/mol?L-1 | 0.5 | 0.5 | 0.5 | 0.5 |
| A | B | C | D | |
| C(CO2) | 3 | 1 | 2 | 2 |
| C(H2) | 2 | 1 | 1 | 2 |
| C(CO) | 1 | 2 | 4 | 3 |
| C(H2O) | 5 | 2 | 0.5 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com